题目内容
 如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为:
如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为:CH3CH2OH
| 浓硫酸 |
| 170℃ |
回答下列问题:
(1)图1中仪器①、②的名称分别为
(2)收集乙烯气体最好的方法是
(3)向溴的四氯化碳溶液中通入乙烯(如图2),溶液的颜色很快褪去,该反应属于
考点:乙醇的消去反应
专题:实验题
分析:(1)根据仪器①②的构造写出仪器①②的名称;
(2)空气的平均分子量为29,乙烯的分子量为28,二者比较接近,不能使用排空气法收集,乙烯不溶于水,可用排水法收集;
(3)乙烯分子中含有碳碳双键,能够与溴的四氯化碳发生加成反应生成1,2-二溴乙烷.
(2)空气的平均分子量为29,乙烯的分子量为28,二者比较接近,不能使用排空气法收集,乙烯不溶于水,可用排水法收集;
(3)乙烯分子中含有碳碳双键,能够与溴的四氯化碳发生加成反应生成1,2-二溴乙烷.
解答:
解:(1)图1中仪器①用于测量反应温度,名称为温度计;仪器②由于盛放乙醇和浓硫酸的混合液,名称为圆底烧瓶,
故答案为:温度计;圆底烧瓶;
(2)乙烯的密度与空气密度接近,不能使用排空气法收集,乙烯不溶于水,可以用排水法水解乙烯,
故答案为:排水集气法;
(3)向溴的四氯化碳溶液中通入乙烯(如图2),乙烯与溴发生加成反应生成1,2-二溴乙烷,所以溶液的颜色很快褪去,反应的化学方程式为:CH2=CH2+Br2→CH2BrCH2Br,故答案为:加成反应;CH2=CH2+Br2→CH2BrCH2Br.
故答案为:温度计;圆底烧瓶;
(2)乙烯的密度与空气密度接近,不能使用排空气法收集,乙烯不溶于水,可以用排水法水解乙烯,
故答案为:排水集气法;
(3)向溴的四氯化碳溶液中通入乙烯(如图2),乙烯与溴发生加成反应生成1,2-二溴乙烷,所以溶液的颜色很快褪去,反应的化学方程式为:CH2=CH2+Br2→CH2BrCH2Br,故答案为:加成反应;CH2=CH2+Br2→CH2BrCH2Br.
点评:本题主要考查了乙烯的实验室制法,题目难度不大,注意掌握常见仪器的干燥及使用方法,明确乙烯的实验室制法及反应原理.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,22.4LCCl4含有NA个分子 |
| B、0.1molAlCl3完全转化为胶体,生成胶体粒子的数目为0.l NA个 |
| C、常温常压下46gNO2和N2O4的混合气体含有3NA个原子 |
| D、0.1molCl2与足量冷的NaOH溶液反应,转移电子数为0.2 NA |
如图所示装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体,该装置可用于( )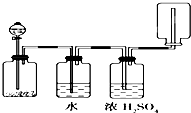

| A、KMnO4分解生成氧气 |
| B、二氧化锰和盐酸生产氯气 |
| C、碳酸钙和盐酸生成二氧化碳 |
| D、锌和盐酸生成氢气 |
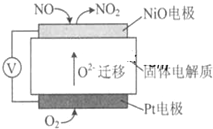 SO2、NOx是大气的主要污染物.
SO2、NOx是大气的主要污染物.