题目内容
4.明矾石的主要成分是K2SO4•Al2(SO4)3•2Al2O3•6H2O,此外还含有少量Fe2O3杂质.利用明矾石制备氢氧化铝的流程如下: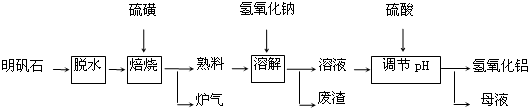
(1)“焙烧”过程中反应的化学方程式为2Al2(SO4)3+3S $\frac{\underline{\;高温\;}}{\;}$ 2Al2O3+9SO2.该反应的氧化剂是Al2(SO4)3.
(2)“溶解”时反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是取最后一次洗涤的滤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净.
(4)“母液”中可回收的物质是K2SO4、Na2SO4.
分析 明矾石经脱水后,在焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S$\frac{\underline{\;高温\;}}{\;}$2Al2O3+9SO2,故生成炉气中含二氧化硫,熟料中含氧化铝、氧化铁、硫酸钾等,加入氢氧化钠和水,氧化铝和氢氧化钠反应生成偏铝酸钠,氧化铁不反应,过滤,滤渣中含氧化铁,滤液中含偏铝酸钠和硫酸钾、氢氧化钠等;用硫酸调节pH,得到氢氧化铝沉淀和硫酸钠、硫酸钾,过滤得母液中含硫酸钾、硫酸钠溶质,以此解答该题.
解答 解:(1)反应中硫元素化合价由Al2(SO4)3中S元素的+6价降低,单质硫中S的化合价升高,令产物中S的化合价为+x价,根据得失电子守恒可知6(6-x)=3(x-0),则x=4,所以生成产物为SO2,则反应的化学方程式为2Al2(SO4)3+3S$\frac{\underline{\;高温\;}}{\;}$2Al2O3+9SO2,Al2(SO4)3化合价降低得电子为氧化剂,
故答案为:9SO2;Al2(SO4)3;
(2)氢氧化钠与氧化铝反应生成偏铝酸钠和水,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O;
(3)Al(OH)3沉淀具有吸附性,可吸附硫酸根离子,通过检验硫酸根离子的方法进行实验,方法为取最后一次洗涤的流出液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净,
故答案为:取最后一次洗涤的滤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净;
(4)根据流程分析可知“母液”中含有硫酸盐中含有K2SO4、Na2SO4,都可回收利用,
故答案为:K2SO4、Na2SO4.
点评 本题考查物质的制备、分离等知识,侧重于学生的分析能力和计算能力的考查,为高考常见题型,难度中等,注意把握物质的相关性质.

| A. | 浓硫酸具有脱水性,因而能使蔗糖炭化 | |
| B. | 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸具有吸水性,因此可用作干燥剂,能干燥氢气、硫化氢、氨气等气体 | |
| D. | 因为浓硫酸在常温下不可与铁或铝反应,因此常温下可用铁制或铝制容器储存浓硫酸 |
| R | ||
| X | Y | Z |
| A. | 可用YO2+Z2+2H2O=H2YO4+2HZ,证明非金属性:Z>Y | |
| B. | 含有Z元素的钠盐溶液都呈中性 | |
| C. | 由非金属性Z>Y可知,最高价氧化物对应的水化物的氧化性:Z>Y | |
| D. | 最简单气态氢化物的热稳定性:R>X |
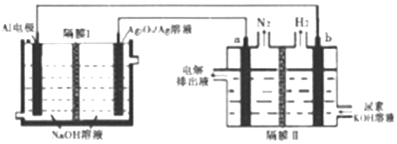
| A. | Ag电极是正极,反应后该电极区溶液pH减小 | |
| B. | 原电池的总反应为:2Al+3Ag2O2+2NaOH═2NaAlO2+3Ag2O+H2O | |
| C. | a电极上的电极反应为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O | |
| D. | 每消耗2.7g铝,理论上a、b两级共产生气体3.36L(标准状况) |
| A. | 向生石灰中滴加浓氨水,可以制备氨气 | |
| B. | 用分液漏斗、烧杯、铁架台可以分离碘的四氯化碳溶液 | |
| C. | 用排饱和硝酸钾溶液的方法可以收集铜与浓硝酸产生的NO2 | |
| D. | 在含少量AlCl3的MgCl2溶液中加人过量MgO,过滤得到MgCl2溶液 |
| A. | C3H2Cl6有四种同分异构体 | |
| B. | 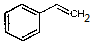 中所有原子可能共平面 中所有原子可能共平面 | |
| C. | 乙醇被酸性KMnO4溶液充分氧化的化学方程式为5CH3CH2OH+2KMnO4+3H2SO4→5CH3CHO+K2SO4+2MnSO4+8H2O | |
| D. | -C3H7和-C2H5O各取代苯分子中的一个氢原子形成的二元取代物的同分异构体有24种 |
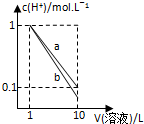
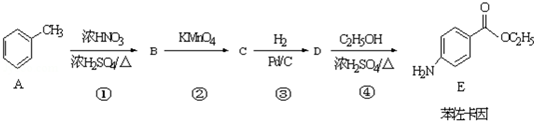
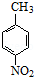 .
.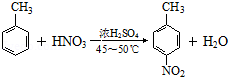 ;反应④的化学方程式为
;反应④的化学方程式为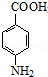 +CH3CH2OH
+CH3CH2OH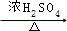
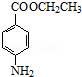 +H2O.
+H2O.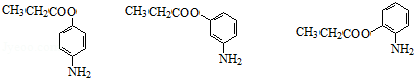 .(任写一种)
.(任写一种) 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题: