题目内容
14.下列关于有机物的说法不正确的是( )| A. | C3H2Cl6有四种同分异构体 | |
| B. | 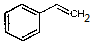 中所有原子可能共平面 中所有原子可能共平面 | |
| C. | 乙醇被酸性KMnO4溶液充分氧化的化学方程式为5CH3CH2OH+2KMnO4+3H2SO4→5CH3CHO+K2SO4+2MnSO4+8H2O | |
| D. | -C3H7和-C2H5O各取代苯分子中的一个氢原子形成的二元取代物的同分异构体有24种 |
分析 A.分子式为C3H2Cl6的有机物可以看作C3Cl8中的两个Cl原子被两个H原子取代,两个H原子可以取代同一碳原子的2个Cl原子,也可以取代不同C原子上的Cl原子,据此书写解答;
B.分子中含C=C和苯环,根据乙烯为平面机构、苯为正六边形结构进行判断共平面原子数;
C.乙醇能被酸性高锰酸钾充分氧化为乙酸;
D.根据-C3H7、-C2H5O异构体及苯环的位置判断异构体的种类即可.
解答 解:A.分子式为C3H2Cl6的有机物可以看作C3Cl8中的两个Cl原子被两个H原子取代,碳链上的3个碳中,两个氢原子取代一个碳上的氯原子,有2种:CCl3-CCl2-CClH2 、CCl3-CH2 -CCl3;分别取代两个碳上的氯原子,有2种:CCl2H-CCl2-CCl2H(两个边上的),CCl2H-CHCl-CCl3 (一中间一边上),共有4种,故A正确;
B. 中连接苯环部分上有12个原子共平面,碳碳双键连接部分有6个原子通过转动碳碳键可以与苯环部分共平面,所以所有原子可能共平面,故B正确;
中连接苯环部分上有12个原子共平面,碳碳双键连接部分有6个原子通过转动碳碳键可以与苯环部分共平面,所以所有原子可能共平面,故B正确;
C.乙醇能被酸性高锰酸钾氧化为乙酸,化学方程式为:5CH3CH2OH+4KMnO4+6H2SO4→5CH3COOH+2K2SO4+4MnSO4+11H2O,故C错误;
D.-C3H7有2种结构,分别为CH3-CH2-CH2-、CH3-CH(CH3)-,-C2H5O有4种结构,分别为:HOCH2CH2-、CH3CH(OH)-、-OCH2CH3、CH3OCH2-,再考虑苯环上相对位置有邻、间、对三种,所以形成的有机物有2×4×3=24种,故D正确;
故选C.
点评 本题考查了同分异构体的书写,有机物结构中共面、共线问题,中等难度,解题关键要搞清取代基的异构体及苯环的位置.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.将2molPCl3和1molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g),达平衡时PCl5为0.4mol,如果此时移走1.0molPCl3和0.5molCl2,在相同温度下再达平衡时PCl5的物质的量是( )
| A. | 0.4mol | B. | 小于0.2mol | ||
| C. | 大于0.2mol | D. | 大于0.2mol,小于0.4mol |
2.配制物质的鼙浓度为0.1mo•L-I的Na2CO3溶液l00mL时,下列操作正确的是( )
| A. | 用托盘天平称取l.06g无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中 | |
| B. | 定容时,若仰视,则所配溶液的浓度将偏高 | |
| C. | 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分 | |
| D. | 在使用容避瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水 |
9.已知某溶液中,已电离的水的浓度为10-13 mol/L,则在此溶液中肯定能大量共存的离子是( )
| A. | K+、Na+、Cl-、SO32- | B. | K+、Na+、NO3-、SO42- | ||
| C. | K+、NH4+、NO3-、SO42- | D. | K+、Mg2+、NO3-、Cl- |
19.水热法制备Fe2O3纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O,关于该反应下列说法正确的是( )
| A. | H2O和S4O62-都是还原产物 | |
| B. | 1mol Fe2+参加反应时,转移2mol电子 | |
| C. | Fe2+、S2O32-都是还原剂 | |
| D. | x=2 |
6.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1mol丙烯酸中含有双键的数目为0.1NA | |
| B. | 1mol/L FeCl3溶液中,阴、阳离子总数大于0.4NA | |
| C. | 12g金刚石中所含的C-C键数为2NA | |
| D. | 18g的D2O与NA个CH3-具有相同的电子数 |
3.下列实验设计及其对应的离子方程式均正确的是( )
| A. | 氢氟酸雕刻玻璃:Si+4HF═SiF4↑+2H2↑ | |
| B. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
4.温度为25℃时,将0.46g钠投入到2000g水中充分反应,假设反应后溶液体积为2000mL,则该溶液的pH为( )
| A. | 1 | B. | 13 | C. | 12 | D. | 10 |