题目内容
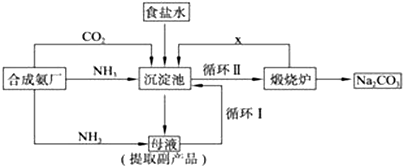
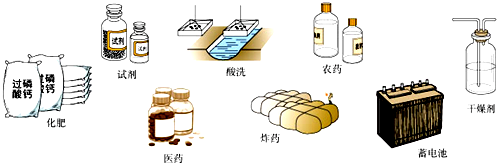
有A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大,甲物质由A、B、D三种元素组成,甲在工业上用途广泛,用途如图,B与C可按原子个数比为1:1或2:1形成的化合物.
(1)画出短周期中E的同主族的另一种元素的原子结构示意图 .
(2)A与B形成的化合物中,含非极性键的化合物的结构式为 .
(3)C与B按原子个数比为1:1形成化合物的电子式是 .
(4)D、E所形成氢化物的稳定性由强到弱的顺序是 、 (填具体的化学式).
(5)由短周期元素组成的某些微粒,如SO2、O3、NO
可互称为等电子体,则与B同周期元素组成的微粒中,能与N
、CS2互称为等电子体的微粒是 (填二种符合要求微粒的名称).
(6)写出工业上由甲制过磷酸钙化学方程式 .

(1)画出短周期中E的同主族的另一种元素的原子结构示意图
(2)A与B形成的化合物中,含非极性键的化合物的结构式为
(3)C与B按原子个数比为1:1形成化合物的电子式是
(4)D、E所形成氢化物的稳定性由强到弱的顺序是
(5)由短周期元素组成的某些微粒,如SO2、O3、NO
- 2 |
- 3 |
(6)写出工业上由甲制过磷酸钙化学方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大,甲物质由A、B、D三种元素组成,甲在工业上用途广泛,用途如图,可知,甲为硫酸,则A为氢元素,B为氧元素,D为硫元素,所以E为氯元素,B与C可按原子个数比为1:1或2:1形成的化合物,则C为钠元素,据此答题.
解答:
解:A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大,甲物质由A、B、D三种元素组成,甲在工业上用途广泛,用途如图,可知,甲为硫酸,则A为氢元素,B为氧元素,D为硫元素,所以E为氯元素,B与C可按原子个数比为1:1或2:1形成的化合物,则C为钠元素,
(1)短周期中E的同主族的另一种元素为氟元素,它的原子结构示意图为 ,
,
故答案为: ;
;
(2)A与B形成的化合物中,含非极性键的化合物为双氧水,它的结构式为H-O-O-H,
故答案为:H-O-O-H;
(3)C与B按原子个数比为1:1形成化合物为过氧化钠,它的电子式是 ,
,
故答案为: ;
;
(4)D、E所形成氢化物为硫化氢和氯化氢,由于氯的非金属性强于硫,所以它们的稳定性由强到弱的顺序是HCl、H2S,
故答案为:HCl、H2S;
(5)SO2、O3、NO2-可互称为等电子体,含有的原子总数相等、价电子总数相等,则与O、F同周期元素组成的微粒中,能与N3-、CS2互称为等电子体,含有3个原子,价电子总数为16的微粒有:二氧化碳、一氧化二氮、二氟化铍,
故答案为:二氧化碳、一氧化二氮、二氟化铍;
(6)工业上由浓硫酸制过磷酸钙化学方程式为Ca3(PO4)2+2H2SO4(浓)=2CaSO4+Ca(H2PO4)2,
故答案为:Ca3(PO4)2+2H2SO4(浓)=2CaSO4+Ca(H2PO4)2.
(1)短周期中E的同主族的另一种元素为氟元素,它的原子结构示意图为
 ,
,故答案为:
 ;
;(2)A与B形成的化合物中,含非极性键的化合物为双氧水,它的结构式为H-O-O-H,
故答案为:H-O-O-H;
(3)C与B按原子个数比为1:1形成化合物为过氧化钠,它的电子式是
 ,
,故答案为:
 ;
;(4)D、E所形成氢化物为硫化氢和氯化氢,由于氯的非金属性强于硫,所以它们的稳定性由强到弱的顺序是HCl、H2S,
故答案为:HCl、H2S;
(5)SO2、O3、NO2-可互称为等电子体,含有的原子总数相等、价电子总数相等,则与O、F同周期元素组成的微粒中,能与N3-、CS2互称为等电子体,含有3个原子,价电子总数为16的微粒有:二氧化碳、一氧化二氮、二氟化铍,
故答案为:二氧化碳、一氧化二氮、二氟化铍;
(6)工业上由浓硫酸制过磷酸钙化学方程式为Ca3(PO4)2+2H2SO4(浓)=2CaSO4+Ca(H2PO4)2,
故答案为:Ca3(PO4)2+2H2SO4(浓)=2CaSO4+Ca(H2PO4)2.
点评:本题主要考查了原子结构示意图、结构式、电子式、元素周期律、等电子体、硫酸的工业应用等知识,中等难度,元素推断是解题的关键,也是本题的难点.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列说法错误的是( )
| A、化学键的断裂和形成是化学反应中能量变化的主要原因 |
| B、放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小 |
| C、化学反应中能量变化,通常主要表现为热量的变化------放热或者吸热 |
| D、凡经加热而发生的化学反应都是吸热反应 |
已知X,Y声是元素周期表中前20号元素:|x-y|=3,X,Y能形成化合物M,下列说法正确的是( )
| A、若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B、若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C、若M属于共价化合物,则该分子中原子个数比可能为1:2 |
| D、若M属于离子化合物,则该化合物中只存在离子键 |