题目内容
已知X,Y声是元素周期表中前20号元素:|x-y|=3,X,Y能形成化合物M,下列说法正确的是( )
| A、若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B、若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C、若M属于共价化合物,则该分子中原子个数比可能为1:2 |
| D、若M属于离子化合物,则该化合物中只存在离子键 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A、若X、Y处于同一周期,原子序数相差3,不能确定X、Y的原子序数,则原子半径不确定;
B、若X和Y处于不同的周期,可以为Na与O或Ca与Cl等;
C、若M属于共价化台物,C与F元素形成CF2=CF2等原子个数比可能为1:2;
D、若M属于离子化合物,Na与O形成的过氧化钠既含有离子键又含有共价键.
B、若X和Y处于不同的周期,可以为Na与O或Ca与Cl等;
C、若M属于共价化台物,C与F元素形成CF2=CF2等原子个数比可能为1:2;
D、若M属于离子化合物,Na与O形成的过氧化钠既含有离子键又含有共价键.
解答:
解:A、若X、Y处于同一周期,原子序数相差3,不能确定X、Y的原子序数,X原子半径可能对于Y,也可能小于Y,故A错误;
B、若X和Y处于不同的周期,可以为Na与O或Ca与Cl等,氧化钠溶于水呈碱性,而氯化钙溶液呈中性,故B错误;
C、若M属于共价化台物,C与F元素形成CF2=CF2等原子个数比可能为1:2,故C正确;
D、若M属于离子化合物,Na与O形成的过氧化钠既含有离子键又含有共价键,故D错误;故选C.
B、若X和Y处于不同的周期,可以为Na与O或Ca与Cl等,氧化钠溶于水呈碱性,而氯化钙溶液呈中性,故B错误;
C、若M属于共价化台物,C与F元素形成CF2=CF2等原子个数比可能为1:2,故C正确;
D、若M属于离子化合物,Na与O形成的过氧化钠既含有离子键又含有共价键,故D错误;故选C.
点评:本题主要考查位置结构性质关系应用,题目难度中等,注意利用列举法进行解答,需要学生对基础知识全面掌握.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
下列叙述中,不正确的是( )
| A、常温下,pH=3的盐酸与pH=11的氨水溶液中水的电离程度相同 |
| B、滴定相同体积和物质的量浓度的盐酸和醋酸,消耗一定物质的量浓度的烧碱溶液的体积相同 |
| C、0.1 mol/L的Na2CO3溶液和0.01 mol/LNaHCO3溶液中离子种类相同,而且都满足关系式:c(Na+)=c(HCO3-)+2c(CO32-)+c(OH-)-c(H+) |
| D、常温下,pH值之和为14的醋酸和NaOH溶液,等体积混合后,溶液pH>7 |
下列解释或结论中,错误的是( )
| A、利用NaOH溶液除去金属铝表面的氧化膜的 |
| B、NaCl溶液与CH3COONH4溶液均呈中性,说明两溶液中水的电离程度相同 |
| C、1mol某醇与足量的钠反应生成22.4L氢气(标况下),该醇为二元醇 |
| D、向KI溶液中滴加氯水和CCl4,振荡,静置后溶液出现分层且下层显紫色,证明Cl2氧化性强于I2 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,8gO2含有4NA个电子 |
| B、1L 1mol/L 的NaClO 溶液中含有ClO-的数目为NA |
| C、标准状况下,22.4L盐酸含有NA个HCl分子 |
| D、1mol Na被完全氧化生成Na2O2,失去2NA个电子 |
下列离子方程式中正确的是( )
| A、稀盐酸滴在石灰石上:CaCO3+2H+═Ca2++H2CO3 |
| B、硝酸银溶液与食盐水的反应:Ag++Cl-═AgCl↓ |
| C、锌与盐酸的反应:Zn+2H++2Cl-═Zn2++2Cl-+H2↑ |
| D、氧化铜与稀硫酸的反应:CuO+2H++SO42-═CuSO4+H2O |
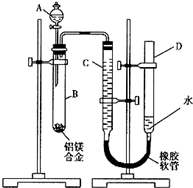 含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案: