题目内容
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 高温下,16.8g Fe与足量水蒸气完全反应失去电子数为0.8NA | |
| B. | 一定条件下Fe粉与足量的浓硫酸反应,转移电子数为3NA | |
| C. | 在1L的碳酸钠溶液中,若c(CO32- )=1mol•L-1,则溶液中Na+的个数为2NA | |
| D. | 含4NA个离子的固体Na2O2溶于水配成1L溶液,所得溶液中c(Na+)=2mol•L-1 |
分析 A、求出铁的物质的量,然后根据铁与水蒸气反应后变为+$\frac{8}{3}$价来分析;
B、铁粉的物质的量不明确;
C、碳酸根是弱酸根,在溶液中会水解;
D、过氧化钠由2个钠离子和1个过氧根构成.
解答 解:A、16.8g铁的物质的量为0.3mol,而铁与水蒸气反应后变为+$\frac{8}{3}$价,故0.3mol铁转移0.8mol电子即0.8NA个,故A正确;
B、铁粉的物质的量不明确,故转移的电子数无法计算,故B错误;
C、碳酸根是弱酸根,在溶液中会水解,导致碳酸根的浓度减少,故当c(CO32- )=1mol•L-1时,溶液中钠离子的浓度大于2mol/L,则物质的量大于2mol,个数大于2NA个,故C错误;
D、过氧化钠由2个钠离子和1个过氧根构成,即1mol过氧化钠中含3NA个离子,故含4NA个离子的Na2O2的物质的量为$\frac{4}{3}$mol,含有的钠离子的物质的量为$\frac{8}{3}$mol,故形成的1L溶液中钠离子的浓度为$\frac{8}{3}$mol/L,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
20.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
| A. | NaCO3溶液(NaHCO3),选用适量NaOH溶液 | |
| B. | NaHCO3溶液(NaCO3),应通入过量CO2气体 | |
| C. | Na2O2粉末(Na2O),将混合物在空气中加热 | |
| D. | 镁粉(铝粉),选用过量的烧碱溶液 |
17.标准状况下,将体积为V L的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm-3.下列说法错误的是( )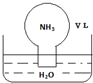

| A. | 水最终会充满整个烧瓶 | |
| B. | 所得溶液的物质的量浓度为$\frac{1}{22.4}$ mol•L-1 | |
| C. | 所得溶液的质量分数为$\frac{17}{22400}$ρ | |
| D. | 所得溶液中,n(NH3•H2O)+n(NH4+)=$\frac{V}{22.4}$mol |
4.下列叙述正确的是( )
| A. | 常温下,pH=5的NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| B. | 在0.1mol•L-1 CH3COONa溶液中:n(OH-)+0.1mol>n(CH3COOH)+n(H+)+n(Na+) | |
| C. | 向AgBr的饱和溶液中加入NaCl固体,有白色固体析出,说明AgCl比AgBr更难溶 | |
| D. | 10mL 0.01mol•L-1 H2SO4溶液与10mL 0.01mol•L-1 NaOH溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=7 |
14.我国的“神州五号”载人飞船已发射成功,“嫦娥”探月工程已正式启动.据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以42He的形式存在.下列说法正确的是( )
| A. | 42He原子核内含有2个质子 | |
| B. | 32He和42He互为同素异形体 | |
| C. | 32He原子核内含有2个中子 | |
| D. | 42He的最外层电子数为4,所以42He具有较强的金属性 |
1.反应2NH3(g)?N2(g)+3H2(g)在密闭容器内进行,已知起始时NH3的物质的量浓度为2.0mol/L,5s后为1.2mol/L,则此段时间内用氨的浓度变化表示该反应的平均速率为( )
| A. | 1.6 mol/(L•s) | B. | 0.16 mol/(L•s) | C. | 0.32mol/(L•s) | D. | 0.8 mol/(L•s) |
18.在两个容积相同的密闭容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定不能具有相同的( )
| A. | 密度 | B. | 颜色 | C. | 原子数 | D. | 分子数 |
19.聚乳酸是一种生物降解塑料,乳酸的结构简式为HOCH(CH3)COOH,下列说法正确的是( )
| A. | 聚乳酸的相对分子质量是72 | |
| B. | 乳酸的分子式是C2H6O3 | |
| C. | 1mol乳酸和适量的金属钠可放出氢气44.8L(标准状况) | |
| D. | 1mol乳酸和少量的碳酸氢钠溶液反应可放出二氧化碳22.4L(标准状况) |
 某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成橙黄色晶体X.为确定其组成,进行如下实验.
某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成橙黄色晶体X.为确定其组成,进行如下实验.