题目内容
18.在两个容积相同的密闭容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定不能具有相同的( )| A. | 密度 | B. | 颜色 | C. | 原子数 | D. | 分子数 |
分析 在同温同压下,相同体积的任何气体含有相同的分子数,HCl、H2和Cl2都是双原子分子,当分子数相等时,原子数一定相等;H2和Cl2的物质的量之比为1:1时相当于HCl,两个容器内的密度相等,但H2和Cl2的物质的量之比不一定为1:1,氯气为黄绿色气体,而HCl为无色气体,颜色一定不相同.
解答 解:同温同压下,氢气、氯气的总体积与HCl体积相等,则H2和Cl2总物质的量与HCl物质的量相等.
A.H2和Cl2的物质的量之比为1:1时相当于HCl,两个容器内的密度相等,但H2和Cl2的物质的量之比不一定为1:1,故两个容器内密度不一定相等,故A不选;
B.氯气为黄绿色气体,而HCl为无色气体,颜色一定不相同,故B选;
C.H2和Cl2总物质的量与HCl物质的量相等,都是双原子分子,当二者分子数相等时,原子数一定相等,故C不选;
D.在同温同压下,相同体积的任何气体含有相同的分子数,故D不选,
故选:B.
点评 本题考查阿伏加德罗定律的应用,注意相关计算公式的运用,注意氢气与氯气物质的量相等时可以相当于为HCl.

练习册系列答案
相关题目
8.除去BaCl2 溶液的少量盐酸,最好选择的试剂是( )
| A. | Ba(OH)2溶液 | B. | BaCO3粉末 | C. | AgNO3溶液 | D. | NaOH溶液 |
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 高温下,16.8g Fe与足量水蒸气完全反应失去电子数为0.8NA | |
| B. | 一定条件下Fe粉与足量的浓硫酸反应,转移电子数为3NA | |
| C. | 在1L的碳酸钠溶液中,若c(CO32- )=1mol•L-1,则溶液中Na+的个数为2NA | |
| D. | 含4NA个离子的固体Na2O2溶于水配成1L溶液,所得溶液中c(Na+)=2mol•L-1 |
6.某实验室制取苯甲酸的过程如下:
(一)如图所示,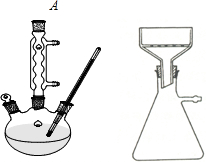
向250mL三颈瓶中加入2.7mL(2.3g)甲苯和100mL水,瓶口装仪器A,加热至沸.从仪器A上口分批加入8.5g高锰酸钾.用少量水(约25mL)将粘在仪器A内壁的高锰酸钾冲洗入烧瓶内.继续煮沸并间歇摇动烧瓶直到甲苯层消失,回流液不再有明显油珠,反应如下:

(二)将反应混合物趁热过滤,用少量热水洗涤滤渣二氧化锰,用玻棒小心搅动(不要使滤纸松动).滤液并倒入400mL烧怀中,将烧杯冷却,然后用浓盐酸酸化,直到苯甲酸全部析出为止;得纯净的苯甲酸质量为1.83g.苯甲酸在不同温度下的溶解度如表:
(1)仪器A的名称是球形冷凝管,(1分)冷却水的进出口方向低进高出
(2)加热前,应先向三颈瓶中加入沸石,其目的是防止暴沸.
(3)反应结束时,溶液还显紫红色,可通过三颈瓶的一个口,向其中加入Na2SO3溶液,发生反应的离子方程式是2MnO4-+3SO32-+H2O=2MnO2+3SO42-+2OH-.(提示:在本实验条件下,高锰酸钾的还原产物是MnO2)
(4)烧杯中的滤液要快速充分冷却,冷却时应将烧杯应放在冷水浴中冷却;然后用浓盐酸酸化,目的是: (用化学方程式表示).
(用化学方程式表示).
(一)如图所示,

向250mL三颈瓶中加入2.7mL(2.3g)甲苯和100mL水,瓶口装仪器A,加热至沸.从仪器A上口分批加入8.5g高锰酸钾.用少量水(约25mL)将粘在仪器A内壁的高锰酸钾冲洗入烧瓶内.继续煮沸并间歇摇动烧瓶直到甲苯层消失,回流液不再有明显油珠,反应如下:

(二)将反应混合物趁热过滤,用少量热水洗涤滤渣二氧化锰,用玻棒小心搅动(不要使滤纸松动).滤液并倒入400mL烧怀中,将烧杯冷却,然后用浓盐酸酸化,直到苯甲酸全部析出为止;得纯净的苯甲酸质量为1.83g.苯甲酸在不同温度下的溶解度如表:
| 温度/℃ | 4 | 18 | 75 |
| 溶解度/[g•(100gH2O)-1] | 0.18 | 0.27 | 2.2 |
(2)加热前,应先向三颈瓶中加入沸石,其目的是防止暴沸.
(3)反应结束时,溶液还显紫红色,可通过三颈瓶的一个口,向其中加入Na2SO3溶液,发生反应的离子方程式是2MnO4-+3SO32-+H2O=2MnO2+3SO42-+2OH-.(提示:在本实验条件下,高锰酸钾的还原产物是MnO2)
(4)烧杯中的滤液要快速充分冷却,冷却时应将烧杯应放在冷水浴中冷却;然后用浓盐酸酸化,目的是:
 (用化学方程式表示).
(用化学方程式表示).
13.下列物质的主要成分正确的是( )
| A. | 赤铁矿:Fe3O4 | B. | 铜绿:Cu2(OH)2CO3 | C. | 磁铁矿:Fe2O3 | D. | 明矾:2KAl(SO4)2 |
3.下列物质在水中的电离方程式错误的是( )
| A. | NH4HCO3═NH4++HCO3- | B. | Ba(NO3)2═Ba2++2NO3- | ||
| C. | Ca(OH)2═Ca2++(OH)2- | D. | KAl(SO4)2═K++Al3++2SO42- |
10.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(l)△H=-483.6 kJ•mol-1,则2molH2(g)和1molO2(g)所含有的总能量比2molH2O(l)所含有的总能量少483.6kJ | |
| B. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 |
7.雾霾给人们的出行带来不便,更对人们的健康带来危害,空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成的视觉障碍的叫霾.当水汽凝结加剧、空气湿度增大时,霾就会转化为雾,下列有关说法不正确的是( )
| A. | 雾霾天车灯照射的光亮通路属于丁达尔现象 | |
| B. | 二氧化碳、氢氧化物和可吸入颗粒物等是雾霾的主要成分 | |
| C. | 寒冷的冬天,餐桌上的火锅冒出的热气是水蒸气 | |
| D. | 减少户外活动,戴上口罩等是有效应对雾霾天气的方法 |
8.下列离子方程式书写不正确的是( )
| A. | SiO2与烧碱溶液作用:SiO2+2OH-═SiO32-+H2O | |
| B. | 向烧碱溶液中通入足量CO2:CO2+OH-═HCO3- | |
| C. | 晶体硅与烧碱溶液作用:Si+2OH-+H2O═SiO32-+2H2↑ | |
| D. | CaCO3溶于稀硝酸中:CO32-+2H+═CO2↑+H2O |