题目内容
1.反应2NH3(g)?N2(g)+3H2(g)在密闭容器内进行,已知起始时NH3的物质的量浓度为2.0mol/L,5s后为1.2mol/L,则此段时间内用氨的浓度变化表示该反应的平均速率为( )| A. | 1.6 mol/(L•s) | B. | 0.16 mol/(L•s) | C. | 0.32mol/(L•s) | D. | 0.8 mol/(L•s) |
分析 5s内氨气浓度变化量为2mol/L-1.2mol/L=0.8mol/L,再根据v=$\frac{△c}{△t}$计算用氨气表示的反应速率.
解答 解:5s内氨气浓度变化量为2mol/L-1.2mol/L=0.8mol/L,用氨气表示的平均反应速率为$\frac{0.8mol/L}{5s}$=0.16 mol/(L•s),
故选:B.
点评 本题考查化学反应速率计算,比较基础,注意对反应速率定义式理解与灵活应用.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
12.不饱和酯类化合物在药物、涂料等应用广泛.下列化合物I的说法,正确的是( )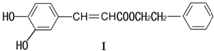
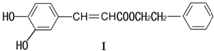
| A. | 遇FeCl3溶液可能显紫色 | |
| B. | 可发生酯化反应和银镜反应 | |
| C. | 能与溴发生取代和加成反应 | |
| D. | 1mol化合物I最多能与2molNaOH反应 |
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 高温下,16.8g Fe与足量水蒸气完全反应失去电子数为0.8NA | |
| B. | 一定条件下Fe粉与足量的浓硫酸反应,转移电子数为3NA | |
| C. | 在1L的碳酸钠溶液中,若c(CO32- )=1mol•L-1,则溶液中Na+的个数为2NA | |
| D. | 含4NA个离子的固体Na2O2溶于水配成1L溶液,所得溶液中c(Na+)=2mol•L-1 |
6.某实验室制取苯甲酸的过程如下:
(一)如图所示,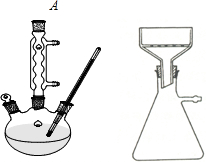
向250mL三颈瓶中加入2.7mL(2.3g)甲苯和100mL水,瓶口装仪器A,加热至沸.从仪器A上口分批加入8.5g高锰酸钾.用少量水(约25mL)将粘在仪器A内壁的高锰酸钾冲洗入烧瓶内.继续煮沸并间歇摇动烧瓶直到甲苯层消失,回流液不再有明显油珠,反应如下:

(二)将反应混合物趁热过滤,用少量热水洗涤滤渣二氧化锰,用玻棒小心搅动(不要使滤纸松动).滤液并倒入400mL烧怀中,将烧杯冷却,然后用浓盐酸酸化,直到苯甲酸全部析出为止;得纯净的苯甲酸质量为1.83g.苯甲酸在不同温度下的溶解度如表:
(1)仪器A的名称是球形冷凝管,(1分)冷却水的进出口方向低进高出
(2)加热前,应先向三颈瓶中加入沸石,其目的是防止暴沸.
(3)反应结束时,溶液还显紫红色,可通过三颈瓶的一个口,向其中加入Na2SO3溶液,发生反应的离子方程式是2MnO4-+3SO32-+H2O=2MnO2+3SO42-+2OH-.(提示:在本实验条件下,高锰酸钾的还原产物是MnO2)
(4)烧杯中的滤液要快速充分冷却,冷却时应将烧杯应放在冷水浴中冷却;然后用浓盐酸酸化,目的是: (用化学方程式表示).
(用化学方程式表示).
(一)如图所示,

向250mL三颈瓶中加入2.7mL(2.3g)甲苯和100mL水,瓶口装仪器A,加热至沸.从仪器A上口分批加入8.5g高锰酸钾.用少量水(约25mL)将粘在仪器A内壁的高锰酸钾冲洗入烧瓶内.继续煮沸并间歇摇动烧瓶直到甲苯层消失,回流液不再有明显油珠,反应如下:

(二)将反应混合物趁热过滤,用少量热水洗涤滤渣二氧化锰,用玻棒小心搅动(不要使滤纸松动).滤液并倒入400mL烧怀中,将烧杯冷却,然后用浓盐酸酸化,直到苯甲酸全部析出为止;得纯净的苯甲酸质量为1.83g.苯甲酸在不同温度下的溶解度如表:
| 温度/℃ | 4 | 18 | 75 |
| 溶解度/[g•(100gH2O)-1] | 0.18 | 0.27 | 2.2 |
(2)加热前,应先向三颈瓶中加入沸石,其目的是防止暴沸.
(3)反应结束时,溶液还显紫红色,可通过三颈瓶的一个口,向其中加入Na2SO3溶液,发生反应的离子方程式是2MnO4-+3SO32-+H2O=2MnO2+3SO42-+2OH-.(提示:在本实验条件下,高锰酸钾的还原产物是MnO2)
(4)烧杯中的滤液要快速充分冷却,冷却时应将烧杯应放在冷水浴中冷却;然后用浓盐酸酸化,目的是:
 (用化学方程式表示).
(用化学方程式表示).
13.下列物质的主要成分正确的是( )
| A. | 赤铁矿:Fe3O4 | B. | 铜绿:Cu2(OH)2CO3 | C. | 磁铁矿:Fe2O3 | D. | 明矾:2KAl(SO4)2 |
10.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(l)△H=-483.6 kJ•mol-1,则2molH2(g)和1molO2(g)所含有的总能量比2molH2O(l)所含有的总能量少483.6kJ | |
| B. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 |