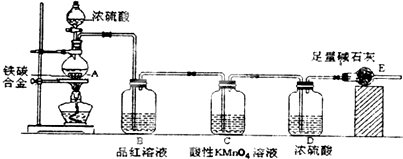
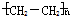题目内容
8.下列有关实验的说法正确的是( )| A. | 向AgI悬浊液中滴加少量NaCl溶液,沉淀转化为白色 | |
| B. | 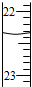 滴定达终点时,如图滴定管的正确读数为23.65 mL | |
| C. | 25℃时,在Mg(OH)2悬浊液中加入少量NH4Cl固体后,c(Mg2+)增大 | |
| D. | 测定溶液的pH时,应先将pH试纸润湿,然后进行检测 |
分析 A.AgI的溶解度比氯化银的溶解度小;
B.滴定管,0刻度在上方,从上到下读数;
C.NH4+结合OH-使氢氧化镁溶解平衡正向移动;
D.先将pH试纸润湿,降低了溶液的浓度.
解答 解:A.沉淀总是向更难溶的方向转化,氯化银溶解度较大,难以生成AgCl沉淀,如生成AgCl沉淀,应加入浓氯化钠溶液,故A错误;
B.滴定管的正确读数为22.32 mL,故B错误;
C.NH4+结合OH-使氢氧化镁溶解平衡正向移动,Mg2+增大,故C正确;
D.测定pH时,为避免误差,pH试纸不能事先用水湿润,故D错误.
故选C.
点评 本题考查较为综合,涉及盐类的水解、滴定管的使用、难溶电解质的溶解平衡以及pH试纸的使用等操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握物质的性质以及实验的严密性、可行性的评价,注意相关基础知识的学习,难度不大.

练习册系列答案
相关题目
18.A+、B2+、C-、D2- 四种离子核外电子排布相同,则这四种离子半径大小顺序是( )
| A. | C->D2->A+>B2+ | B. | B2+>A+>C->D2- | C. | B2+>A+>D2->C- | D. | D2->C->A+>B2+ |
19.在光照条件下,将等物质的量的甲烷和氯气混合充分反应后,得到产物的物质的量最大的是( )
| A. | CH3Cl | B. | CHCl3 | C. | CCl4 | D. | HCl |
16.下列鉴别方法正确的是( )
| A. | 用澄清石灰水鉴别CO2和SO2 | |
| B. | 用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 用CO2鉴别NaAlO2溶液和NaClO溶液 | |
| D. | 用Ba(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液 |
3.元素性质呈周期性变化的根本原因是( )
| A. | 最外层电子数呈周期性变化 | B. | 元素的相对原子质量逐渐增大 | ||
| C. | 核电荷数逐渐增大 | D. | 核外电子排布呈周期性变化 |
13.短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A. | 元素X 的简单气态氢化物的热稳定性比W 的弱 | |
| B. | 原子半径的大小顺序:rY>rZ>rW>rX | |
| C. | 化合物YX、ZX2、WX3 中化学键的类型相同 | |
| D. | 最高价氧化物对应水化物的酸性:W比Z 的弱 |
18.将①中溶液逐滴滴入②中,预测的现象与实际相符的是( )
| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生大量红棕色气体 |
| C | 氯化铁溶液 | 苯酚水溶液 | 溶液变成紫色 |
| D | 氨水 | 氯化铝溶液 | 立即生成白色沉淀,最终沉淀逐渐溶解 |
| A. | A | B. | B | C. | C | D. | D |
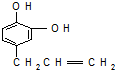

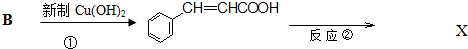
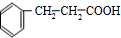 .反应①的化学方程式为:
.反应①的化学方程式为: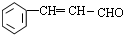 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$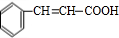 +Cu2O+2H2O.
+Cu2O+2H2O.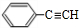 $→_{催化剂}^{HCl}$
$→_{催化剂}^{HCl}$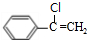 $→_{一定条件}^{CO、H_{2}}$
$→_{一定条件}^{CO、H_{2}}$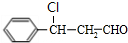 $→_{△}^{NaOH/醇}$
$→_{△}^{NaOH/醇}$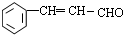 .
.