题目内容
3.元素性质呈周期性变化的根本原因是( )| A. | 最外层电子数呈周期性变化 | B. | 元素的相对原子质量逐渐增大 | ||
| C. | 核电荷数逐渐增大 | D. | 核外电子排布呈周期性变化 |
分析 元素原子的核外电子排布的周期性变化导致元素性质(金属性和非金属性,原子半径,化合价等)的周期性变化,以此来解答.
解答 解:A.同一周期电子层数相同,不是周期性变化,故A错误;
B.随着原子序数的递增,元素的原子的相对原子质量增大,但不呈现周期性的变化,则不能决定元素性质出现周期性变化,故B错误;
C.元素的核电荷数逐渐增大,不体现周期性,不是元素性质周期性变化的根本原因,故C错误;
D.原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素周期律及实质为解答的关键,侧重分析与应用能力的考查,注意结构决定性质的应用,题目难度不大.

练习册系列答案
相关题目
13.下列说法中,正确的是( )
| A. | 卤代烃在NaOH的醇溶液中共热均能发生消去反应生成烯烃 | |
| B. | 凡是能发生银镜反应的物质都属于醛类 | |
| C. | 能与FeCl3溶液作用显紫色的有机物一般含有酚羟基 | |
| D. | 酯类水解均能生成含相同碳原子数的羧酸和醇 |
11.用溴水除去甲烷气体中的少量乙烯,其原理为乙烯能与溴发生( )
| A. | 取代反应 | B. | 加成反应 | C. | 水解反应 | D. | 聚合反应 |
8.下列有关实验的说法正确的是( )
| A. | 向AgI悬浊液中滴加少量NaCl溶液,沉淀转化为白色 | |
| B. | 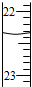 滴定达终点时,如图滴定管的正确读数为23.65 mL | |
| C. | 25℃时,在Mg(OH)2悬浊液中加入少量NH4Cl固体后,c(Mg2+)增大 | |
| D. | 测定溶液的pH时,应先将pH试纸润湿,然后进行检测 |
12.下列说法错误的是( )
| A. | 硅太阳能电池、计算机芯片、光导纤维都用到硅单质 | |
| B. | 水晶镜片、石英钟表、玛瑙手镯含有SiO2 | |
| C. | 水泥路桥、门窗玻璃、砖瓦、陶瓷餐具所用材料为硅酸盐 | |
| D. | 熔融烧碱时不能使用普通玻璃坩埚、石英坩埚和陶瓷坩埚 |
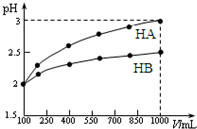 已知100mL pH=2的两种一元酸HA和HB,稀释过程中pH与溶液体积的关系如图所示.
已知100mL pH=2的两种一元酸HA和HB,稀释过程中pH与溶液体积的关系如图所示. 如图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去).其中A是单质,D在常温下呈气态,F可用作氮肥.
如图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去).其中A是单质,D在常温下呈气态,F可用作氮肥.