��Ŀ����
19��Na2CO3����ȡ������Na2CO3��NaHCO3�ۺ�ʵ��̽����1���ҹ���ѧ�Һ�°�ĸ����Ĵ����������գ����������̿ɼ�Ҫ��ʾ��ͼ��
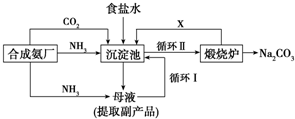
��������ʳ��ˮ������ͨ��������NH3��CO2���������������ͨCO2��ͨNH3��ԭ��������CO2��NaCl��Һ�е��ܽ�Ⱥ�С��NH3��ˮ���ܽ�Ƚϴ���ͨ��NH3ʹʳ��ˮ�ʼ��ԣ��ܹ����մ���CO2���壬�����ϸ�Ũ�ȵ�HCO3-����������NaHCO3���壮
��д���������з�Ӧ�Ļ�ѧ����ʽNH3+H2O+CO2+NaCl�TNH4Cl+NaHCO3����
��ijʵ��С��̽��Na2CO3��NaHCO3�����ʣ�����ʵ������ʢ�����ֹ�����Լ�ƿ��ʧ�˱�ǩ�����ǣ������ȶԹ���A��B���м�����ͨ��ʵ���������̽����
��2���ֱ���ȹ���A��B�����ֹ���A���Ȳ�����������ʹ����ʯ��ˮ����ǣ�A���ȷֽ�Ļ�ѧ����ʽΪ2NaHCO3$\frac{\underline{\;����\;}}{\;}$Na2CO3+CO2��+H2O��
��3����ȡ���ֹ����2g���ֱ��������С�ձ��У��ٸ���10mL����ˮ���������¶ȱ仯�����������ܽ⣬�ָ������£���������Һ�и�����2�η�̪��Һ��
�ٷ���Na2CO3������ȫ�ܽ⣬��NaHCO3������ʣ�࣬�ɴ˵ó����ۣ���ͬ�¶��£�Na2CO3��NaHCO3������ˮ��
��ͬѧ�������ձ��л��۲쵽�����������У�ʢ��Na2CO3���ձ��г��ֵ�������b��d������ĸ��ţ���
a����Һ�¶��½�
b����Һ�¶�����
c�������̪���dz��ɫ
d�������̪��ʺ�ɫ
��4��ͬѧ�ǽ����ֹ���ֱ����Ƴ�0.5mol•L-1����Һ���������������Է�Ӧ��������Ԥ�⣺
| ʵ�鷽�� | Ԥ������ | Ԥ������ |
| ����1����2mL Na2CO3��Һ�еμ�1mL 0.5mol•L-1 CaCl2��Һ | �а�ɫ���� | Na2CO3��Һ�е�CO32-Ũ�Ƚϴ�����CaCl2������Ӧ��Ca2++CO32-�TCaCO3�� �����ӷ���ʽ�� |
| ����2����2mL NaHCO3��Һ�еμ�1mL 0.5mol•L-1CaCl2��Һ | �ް�ɫ���� | NaHCO3��Һ�е�CO32-Ũ�Ⱥ�С��������CaCl2��Ӧ |
���� ��1��������CO2��NaCl��Һ�е��ܽ�Ⱥ�С��NH3��ˮ���ܽ�Ƚϴ���ͨ��NH3ʹʳ��ˮ�ʼ��ԣ��ܹ����մ���CO2���壬�����ϸ�Ũ�ȵ�HCO3-��
���Ƽ��ԭ��Ϊ������������̼�ͱ����Ȼ��ƣ��������еõ�����̼�����ƣ�
��2��̼�����ȶ��������ѷֽ⣬̼���������ȶ��Բ�����ֽ⣬���ɶ�����̼���壬������̼���������Ʒ�Ӧ����̼��Ƴ�����
��3���ٳ����£�ͬ������ͬ������ܼ���Na2CO3������ȫ�ܽ⣬��NaHCO3������ʣ�࣬˵��Na2CO3��NaHCO3���ܣ�
��̼�����ܽ���̷��ȣ�̼����Ϊǿ�������Σ�ˮ��ʹ��Һ�ʼ��ԣ�
��4��̼�����ܺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ�CaCl2��NaHCO3��Һ��Ӧ����̼��Ƴ����Ͷ�����̼���壮
��� �⣺��1���ٰ�����������ˮ����������̼����ˮ����ͨ�백������Һ�ʼ��ԣ���ͨ�������̼�����֮�����ת��ΪHCO3-��
�ʴ�Ϊ������CO2��NaCl��Һ�е��ܽ�Ⱥ�С��NH3��ˮ���ܽ�Ƚϴ���ͨ��NH3ʹʳ��ˮ�ʼ��ԣ��ܹ����մ���CO2���壬�����ϸ�Ũ�ȵ�HCO3-����������NaHCO3���壻
���ڳ����ذ�����������̼��ˮ���Ȼ��Ʒ�����Ӧ����̼�����ƺ��Ȼ�泥���Ӧ����ʽΪNH3+H2O+CO2+NaCl�TNH4Cl+NaHCO3����
�ʴ�Ϊ��NH3+H2O+CO2+NaCl�TNH4Cl+NaHCO3����
��2��̼�����ȶ��������ѷֽ⣬̼���������ȶ��Բ�����ֽ⣬���ɶ�����̼���壬���ɵ�CO2����ͨ�����ʯ��ˮ�з�����Ӧ��CO2+Ca��OH��2=CaCO3��+H2O������̼��Ƴ�������ǣ���AΪ̼�����ƣ�A�ֽⷴӦ����ʽΪ2NaHCO3 $\frac{\underline{\;����\;}}{\;}$Na2CO3+CO2��+H2O��
�ʴ�Ϊ��2NaHCO3 $\frac{\underline{\;����\;}}{\;}$Na2CO3+CO2��+H2O��
��3���ٳ�ȡ���ֹ����2g���ֱ��������С�ձ��У��ٸ��μ�10mL����ˮ���������¶ȱ仯�����������ܽ⣬���ָ������º���Na2CO3������ȫ�ܽ⣬��NaHCO3������ʣ�࣬˵����ͬ�����¶��£�ͬ���������ֹ�����ͬ������ܼ��У�Na2CO3��NaHCO3������ˮ��
�ʴ�Ϊ��ͬ�¶��£�Na2CO3��NaHCO3������ˮ��
��a��̼�����ܽ����Ϊ���ȹ��̣���a����
b��̼�����ܽ���̷��ȣ��¶����ߣ���b��ȷ��
c��̼����Ϊǿ�������Σ�ˮ����Һ�ʼ��ԣ������̪��ʺ�ɫ����c����
d��̼����Ϊǿ�������Σ�ˮ����Һ�ʼ��ԣ�̼�����׳ƴ�������̪��ʺ�ɫ����d��ȷ��
�ʴ�Ϊ��b��d��
��4������2��CaCl2��NaHCO3��Һ��Ӧ���ɳ��������壬��֪������̼��ƣ������Ƕ�����̼����Ӧ����ʽΪ��CaCl2+2NaHCO3=CaCO3��+2NaCl+CO2��+H2O�����ӷ�ӦΪCa2++2HCO3-=CaCO3��+CO2��+H2O��
�ʴ�Ϊ��Ca2++2HCO3-=CaCO3��+CO2��+H2O��
���� ���⿼������ʵ�鷽������ƣ�Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ��ʵ���������Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��Na2CO3��NaHCO3�����Լ���ط�Ӧ�ķ���ʽ����д���״���Ϊ��4��������������Ϣ��֪CaCl2��NaHCO3��Һ�ɷ�����Ӧ��CaCl2+2NaHCO3=CaCO3��+2NaCl+CO2��+H2O����Ŀ�ѶȲ���

| A�� | 0.4 mol/L | B�� | 0.2mol/L | C�� | 0.1mol/L | D�� | 0.05mol/L |
| A�� | ��ѧ��Ӧ��һ�����������仯 | |
| B�� | ����Ӧ��Ũ�ȣ�����Ӱٷ�������ѧ��Ӧ����һ������ | |
| C�� | �����¶ȣ�����Ӱٷ�������ѧ��Ӧ����һ������ | |
| D�� | һ��ʹ�ô������Խ��ͷ�Ӧ�Ļ�ܣ��������Ӱٷ������Ӷ���߷�Ӧ���ת���� |
| A�� | ���� | B�� | ��ˮ | C�� | ���� | D�� | ����KMnO4 |
| A�� | �ܼ������죬�õ��ľ������Ҳ�ϴ� | |
| B�� | ��ѹ���˿ɹ��˽�״������ҽ�Ϊ���� | |
| C�� | ��0.1 mol•L-1һԪ��BOH��Һ��pH=10������֪BOH��Һ��BOH�TB++OH- | |
| D�� | ��0.1 mol•L-1һԪ��HA��Һ��pH=3������֪NaA��Һ��A-+H2O?HA+OH- |
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol����Ӧ����l0min��ﵽƽ�⣮��CO��ƽ��ת����=60%��
��2�������£�HR���ᣩ��ҺpH=3��MOH�������ҺpH=11�����ߵ������Ϻ���Һ�Լ��ԣ�������Һ�бض���һ�������ܷ���ˮ�⣬��ˮ�ⷴӦ�����ӷ���ʽM++H2O?MOH+H+
��3��25��ʱ��pH=0��HCl��0.1mol/L��HCl��0.01mol/L��NaOH��pH=14��NaOH������Һ����ˮ���������C��H+��ˮ ֮��Ϊ1��10��100��1��
��4����֪25��ʱ�����볣��Ka��HF��=3.6��10-4����0.1mol•L-1 HF��Һ��c��H+��=6��10-3mol•L-1
��5�����¶�t��ʱ��pH=3��ijˮ��Һ��c��OH-��=10-8 mol/L���ڴ��¶���5��10-5mol/LBa��OH��2��Һ��pH=7��
| A�� | H2��O2��Ӧ����ˮ | B�� | пƬͶ��ϡ������ | ||
| C�� | KMnO4���ȷֽ���ȡO2 | D�� | NH3��HCl�������ɰ��̣�NH4Cl�� |
| A�� | 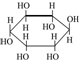 ���������Ϊͬϵ�� ���������Ϊͬϵ�� | |
| B�� | �߾���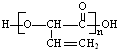 �� ��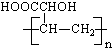 �ĵ�����ͬ �ĵ�����ͬ | |
| C�� | ��ϵͳ��������������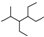 ������Ϊ2-��-3��4-�һ����� ������Ϊ2-��-3��4-�һ����� | |
| D�� | �����ʵ����ļ����������ȫȼ��ʱ����������ȣ����ɵ�CO2����Ҳ��� |