题目内容
19.已知电离平衡常数:H2CO3>HClO>HCO3-.下列离子反应方程式正确的是( )①NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O═2HClO+CO32-
②Na2CO3溶液中加入HClO溶液:CO32-+HClO═HCO3-+ClO-
③等物质的量的Cl2与Na2CO3溶液恰好反应:Cl2+CO32-+H2O═HCO3-+Cl-+HClO
④Cl2通入NaHCO3溶液中:Cl2+2HCO3-═2CO2↑+Cl-+ClO-+H2O.
| A. | ②④ | B. | ①③ | C. | ②③ | D. | ①④ |
分析 电离常数越大物质酸性越强,已知电离平衡常数:H2CO3>HClO>HCO3-,则酸性强弱顺序为:H2CO3>HClO>HCO3-,结合反应中强酸制备弱酸的规律解答.
解答 解:①H2CO3>HClO>HCO3-,则NaClO溶液中通入少量二氧化碳反应生成次氯酸和碳酸氢钠,故①错误;
②次氯酸酸性强于碳酸氢钠弱于碳酸,依据强酸制备弱酸规律,Na2CO3溶液中加入HClO溶液:CO32-+HClO═HCO3-+ClO-,故②正确;
③氯气与水反应生成氯化氢和次氯酸,氯化氢与碳酸钠反应生成氯化钠、碳酸氢钠和水,次氯酸与碳酸氢钠不反应,则离子方程式::Cl2+CO32-+H2O═HCO3-+Cl-+HClO,故③正确;
④Cl2通入NaHCO3溶液中,氯气与水反应生成盐酸和次氯酸,盐酸能够与碳酸氢钠反应生成氯化钠和水、二氧化碳,次氯酸酸性弱于碳酸,所以与碳酸氢钠不反应,应以次氯酸分子形式存在,故④错误;
故选:C.
点评 本题考查了离子方程式的书写正误判断,依据电离常数判断酸性强弱,明确强酸制备弱酸规律是解题关键,题目难度中等.

练习册系列答案
相关题目
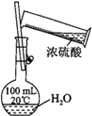
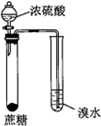
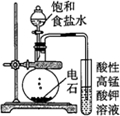
9.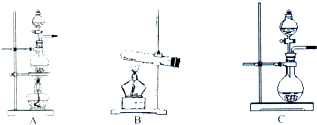 如表是实验室制备气体的有关内容:
如表是实验室制备气体的有关内容:
(1)上述气体中,从反应中有无电子转移的角度看,明显不同于其他气体的是NH3,写出实验室制取该气体的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)根据表中所列实验原理,从如图装置中选择合适的发生装置,将其编号填入上表的空格中.
(3)若用上述制备O2的装置制备NH3,应选择的试剂为浓氨水和氢氧化钠(或生石灰等).
(4)在浓CaCl2溶液中通人NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是NH3,制取纳米级碳酸钙的化学方程式为CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl.试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级取少量样品和水混合形成分散系,用一束光从侧面照射,若出现光亮的通路,则证明样品是纳米级,否则不是.
(5)制备Cl2需用8mol•L-1的盐酸100mL,现用12mol•L-1的盐酸来配制.
①需要用量筒量取12mol•L-1的盐酸的体积为66.7mL;
②实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号)ACFGH.
A.100mL量筒B.托盘天平C.玻璃棒D.50mL容量瓶
E.10mL量筒F.胶头滴管G.100mL烧杯H.100mL容量瓶
③下列实验操作中.不正确的是BC(填写标号).
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加人蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次.
 如表是实验室制备气体的有关内容:
如表是实验室制备气体的有关内容:| 编号 | 实验内容 | 实验原理 | 发生装置 |
| ① | 制氧气 | H2O2→O2 | C |
| ② | 制氨气 | NH4Cl→NH3 | B |
| ③ | 制氯气 | HCl→Cl2 | A或C |
(2)根据表中所列实验原理,从如图装置中选择合适的发生装置,将其编号填入上表的空格中.
(3)若用上述制备O2的装置制备NH3,应选择的试剂为浓氨水和氢氧化钠(或生石灰等).
(4)在浓CaCl2溶液中通人NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是NH3,制取纳米级碳酸钙的化学方程式为CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl.试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级取少量样品和水混合形成分散系,用一束光从侧面照射,若出现光亮的通路,则证明样品是纳米级,否则不是.
(5)制备Cl2需用8mol•L-1的盐酸100mL,现用12mol•L-1的盐酸来配制.
①需要用量筒量取12mol•L-1的盐酸的体积为66.7mL;
②实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号)ACFGH.
A.100mL量筒B.托盘天平C.玻璃棒D.50mL容量瓶
E.10mL量筒F.胶头滴管G.100mL烧杯H.100mL容量瓶
③下列实验操作中.不正确的是BC(填写标号).
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加人蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次.
10.自由能的变化(△G)是反应方向判断的复合判据:△G=△H-T△S,△G<0时反应正向自发进行.已知某化学反应其△H=-122kJ•mol-1,△S=231J/(mol•K),则此反应在下列哪种情况下可自发进行( )
| A. | 在任何温度下都能自发进行 | B. | 在任何温度下都不能自发进行 | ||
| C. | 仅在高温下自发进行 | D. | 仅在低温下自发进行 |
7.下列除去杂质的方法正确的是( )
| A. | 除去KCl溶液中的少量K2CO3:加入适量的盐酸 | |
| B. | 除去CO2中的少量HCl:通入NaOH溶液 | |
| C. | 除去NaCl溶液中的少量MgCl2:加入适量KOH溶液,过滤 | |
| D. | 除去N2中的少量O2:通过灼热的CuO粉末 |
14.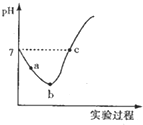 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,整个实验过程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,整个实验过程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,整个实验过程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,整个实验过程中溶液的pH变化曲线如图所示,下列叙述正确的是( )| A. | 实验过程中可用pH试纸测定溶液的pH | |
| B. | a点的溶液中:C(H+)=c(Cl-)+c(HCl0)+c(OH-) | |
| C. | c 点所示溶液中;c(Na+)=2c(ClO )+c(HCIO) | |
| D. | 由a点到b点的过程中,溶液中$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小 |
4.化学与生产生活密切相关,下列说法不正确的是( )
| A. | 食盐可以作为调味剂,也可以调节体液电解质平衡 | |
| B. | 食品保鲜膜、塑料水杯等生活用品的主要成分是聚乙烯 | |
| C. | 化工生产中煤的干馏、石油的分馏、天然气生产甲醇均属于化学变化 | |
| D. | 高铁车厢材料大部分采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强 |
11.分子式为C9H10O2,能与NaHCO3溶液反应放出CO2,且苯环上一氯代物有两种的有机物有(不考虑立体异构)( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
9.加入少许下列一种物质,不能使溴水颜色显著变浅的是( )
| A. | Mg粉 | B. | KOH溶液 | C. | KI溶液 | D. | CCl4 |