题目内容
20.现有A、B、C、D、E、五种短周期元素,它们的原子序数依次增大.A组成的单质是最轻的气体;B的原子最外层电子数为次外层的两倍; D为第三周期元素中原子半径最大的元素;C和D两种元素核外电子总数之和为19;E元素的最高价氧化物对应水化物酸性最强.据此信息,回答下列问题:(1)写出含有18个中子的E的一种原子符号1735Cl,画出C的原子结构示意图
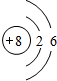 .
.(2)由B和C组成的AB2型化合物属于共价化合物(填“离子”或“共价”),该化合物中含有共价键(填“离子键”或“共价键”或“离子键和共价键”).
(3)由B、C、D三种元素组成的化合物的化学式是Na2CO3,其物质分类属于盐(填“酸”或“碱”或“盐”).
分析 现有A、B、C、D、E、五种短周期元素,它们的原子序数依次增大.A组成的单质是最轻的气体,则A为H元素;B的原子最外层电子数为次外层的两倍,由于最外层电子数不超过8,原子只能有2个电子层,最外层电子数为4,故B为碳元素; D为第三周期元素中原子半径最大的元素,则D为Na;C和D两种元素核外电子总数之和为19,则C为O元素;E元素的最高价氧化物对应水化物酸性最强,则E为Cl.
解答 解:现有A、B、C、D、E、五种短周期元素,它们的原子序数依次增大.A组成的单质是最轻的气体,则A为H元素;B的原子最外层电子数为次外层的两倍,由于最外层电子数不超过8,原子只能有2个电子层,最外层电子数为4,故B为碳元素; D为第三周期元素中原子半径最大的元素,则D为Na;C和D两种元素核外电子总数之和为19,则C为O元素;E元素的最高价氧化物对应水化物酸性最强,则E为Cl.
(1)E为Cl元素,含有18个中子的原子符号为1735Cl,C为O元素,原子结构示意图为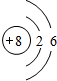 ,
,
故答案为:1735Cl;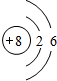 ;
;
(2)由B和C组成的AB2型化合物为CO2,属于共价化合物,该化合物中含有共价键,
故答案为:共价;共价键;
(3)由C、O、Na三种元素组成的化合物的化学式是Na2CO3等,其物质分类属于盐,
故答案为:Na2CO3;盐.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,注意对化学用语与元素化合物知识的掌握,有利于基础知识的巩固.

练习册系列答案
相关题目
16.下列有关实验正确的是( )
| A. |  如图:证明酸性:HNO3>H2CO3>H2SiO3 | |
| B. |  如图:实验室制备氨气 | |
| C. |  如图:实验室制备乙酸乙酯 | |
| D. |  如图:检验浓硫酸与蔗糖反应产生的二氧化硫 |
11.An+、Bn-、C 3种短周期元素的粒子具有相同的电子层结构,则关于它们的叙述正确的是( )
| A. | 原子序数:C>B>A | B. | 离子半径:Bn-<An+ | ||
| C. | C是稀有气体元素的原子 | D. | 原子半径:A<B |
5.如图中的有机化合物可能发生的化学反应有( )

①加成 ②氧化 ③加聚 ④取代.

①加成 ②氧化 ③加聚 ④取代.
| A. | ①② | B. | ①③④ | C. | ①②④ | D. | ①②③④ |
12.现有A、B、C、D四种金属片,
①把A、B用导线连接后同时浸入稀硫酸中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸中,D发生还原反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.
上述四种金属的活动性顺序为( )
①把A、B用导线连接后同时浸入稀硫酸中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸中,D发生还原反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.
上述四种金属的活动性顺序为( )
| A. | A>B>C>D | B. | C>A>B>D | C. | D>B>C>A | D. | B>A>C>D |
9.下列过程中,共价键被破坏的是( )
①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水 ⑤冰融化⑥NH4Cl受热分解 ⑦氢氧化钠熔化 ⑧(NH4)2SO4溶于水.
①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水 ⑤冰融化⑥NH4Cl受热分解 ⑦氢氧化钠熔化 ⑧(NH4)2SO4溶于水.
| A. | ①④⑥⑦ | B. | ④⑥⑧ | C. | ①②④⑤ | D. | ④⑥ |
10.25℃,加水将10mL pH=11的氨水稀释至1L,则下列判断中正确的是( )
| A. | 稀释后溶液的pH=9 | |
| B. | 稀释过程中,溶液中所有离子的浓度均减小 | |
| C. | 稀释后溶液中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}.{H}_{2}O)}$减小 | |
| D. | 该氨水稀释前后中和盐酸的能力相同 |

 ,
, +CO2+H2O→
+CO2+H2O→ +NaHCO3,
+NaHCO3, +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$ +3H2O.
+3H2O.