题目内容
9.下列过程中,共价键被破坏的是( )①碘升华 ②溴蒸气被木炭吸附 ③酒精溶于水 ④HCl气体溶于水 ⑤冰融化⑥NH4Cl受热分解 ⑦氢氧化钠熔化 ⑧(NH4)2SO4溶于水.
| A. | ①④⑥⑦ | B. | ④⑥⑧ | C. | ①②④⑤ | D. | ④⑥ |
分析 一般来说,非金属元素之间形成共价键,由共价键形成的物质在溶于水、化学变化中共价键被破坏,以此来解答.
解答 解:①碘升华,只破坏分子间作用力,故不选;
②溴蒸气被木炭吸附,只破坏分子间作用力,故不选;
③酒精溶于水,不能发生电离,只破坏分子间作用力,故不选;
④HCl气体溶于水,H-Cl共价键断裂,发生电离,故选;
⑤冰融化,破坏分子间作用力、氢键,故不选;
⑥NH4Cl受热分解生成氨气和HCl,离子键、共价键均破坏,故选;
⑦氢氧化钠熔化,发生电离,只破坏离子键,故不选;
⑧(NH4)2SO4溶于水,发生电离,只破坏离子键,故不选;
故选D.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
17.相同物质的量的下列有机物,充分燃烧,消耗氧气量相同的是( )
| A. | C3H4和C2H6 | B. | C2H2和C6H6 | C. | C3H6O和C3H8O2 | D. | C3H8O和C4H8O2 |
14.元素A的阳离子aAm+与元素B的阴离子bBn-具有相同的电子层结构.以下关于A、B元素性质的比较中,正确的是( )
①原子序数:A>B
②离子半径:aAm+<bBn-
③原子半径:A<B
④元素所在的周期序数:A>B
⑤A的最高正价与B的最低负价的绝对值相等
⑥b=a+m-n.
①原子序数:A>B
②离子半径:aAm+<bBn-
③原子半径:A<B
④元素所在的周期序数:A>B
⑤A的最高正价与B的最低负价的绝对值相等
⑥b=a+m-n.
| A. | ②③④ | B. | ④⑤⑥ | C. | ②⑤⑥ | D. | ①②④ |
1.下列叙述正确的是( )
| A. | 非金属与金属化合形成离子化合物 | |
| B. | 含有共价键的化合物都是共价化合物 | |
| C. | 非极性键只存在于双原子单质分子里 | |
| D. | 共价化合物中一定存在极性共价键 |
18.分析表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是( )
| “嫦娥一号”发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1 ②2H2(l)+O2(l)═2H2O(g)△H=-482.6kJ•mol-1 |
| 北京奥运会“祥云”火炬燃料 | 丙烷(C3H8) | ③C3H8(l)+5O2(g)═3CO2(g)+4H2O(g)△H=-2013.8kJ•mol-1 ④C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2221.5kJ•mol-1 |
| A. | 571.6 kJ•mol-1,2221.5kJ•mol-1 | B. | 241.3 kJ•mol-1,2013.8 kJ•mol-1 | ||
| C. | 285.8 kJ•mol-1,2013.8 kJ•mol-1 | D. | 285.8 kJ•mol-1,2221.5 kJ•mol-1 |
19.某有机物2.3克,完全燃烧后的产物依次通过浓硫酸与NaOH溶液,分别增重2.7克与4.4克,该有机物的分子式是( )
| A. | C2H6O | B. | C2H4O | C. | C2H6 | D. | C2H4 |
 .
.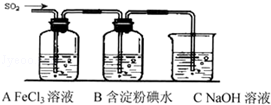 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示: