题目内容
12.现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸中,A上有气泡产生;
②把C、D用导线连接后同时浸入稀硫酸中,D发生还原反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.
上述四种金属的活动性顺序为( )
| A. | A>B>C>D | B. | C>A>B>D | C. | D>B>C>A | D. | B>A>C>D |
分析 ①A上有气泡产生,说明A为正极,则金属A的活泼性较弱;
②D发生还原反应,则D为原电池的正极,则金属D的活泼性小于C;
③电子流动方向为A→导线→C,则电流方向从C流向A,故C为正极、A为负极,活泼性A>C.
解答 解:①把A、B用导线连接后同时浸入稀硫酸中,A上有气泡产生,说明A为该原电池的正极、B为负极,金属活泼性:A<B;
②把C、D用导线连接后同时浸入稀硫酸中,D发生还原反应,说明D为原电池的正极、C为负极,泽尔金属活动性:C>D;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C,说明A失去电子、C得到电子,则A为负极、C为正极,则金属活动性:A>C;
根据分析可知,金属活动性顺序为:B>A>C>D,
故选D.
点评 本题考查了原电池工作原理及其应用,题目难度不大,正确判断原电池的两极为解答关键,注意熟练掌握原电池工作原理,试题侧重基础知识的考查,培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
相关题目
7.下列说法不正确的是( )
| A. | 在25℃时,将c mol•L-1的醋酸溶液与0.02mol•L-1NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=$\frac{2×{10}^{-9}}{c-0.02}$ | |
| B. | 0.1 mol•L-1醋酸溶液中:c(H+)2=c (H+)•c(CH3COO-)+KW | |
| C. | 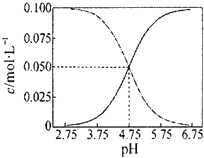 常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 等体积等物质的量浓度的CH3COONa(aq)与NaCl(aq)中离子总数大小:N前>N后 |
17.相同物质的量的下列有机物,充分燃烧,消耗氧气量相同的是( )
| A. | C3H4和C2H6 | B. | C2H2和C6H6 | C. | C3H6O和C3H8O2 | D. | C3H8O和C4H8O2 |
1.下列叙述正确的是( )
| A. | 非金属与金属化合形成离子化合物 | |
| B. | 含有共价键的化合物都是共价化合物 | |
| C. | 非极性键只存在于双原子单质分子里 | |
| D. | 共价化合物中一定存在极性共价键 |
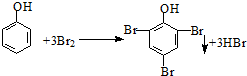 .
.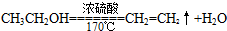 .
.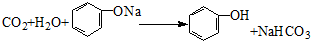 .
.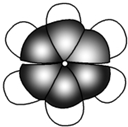 下列给出了四种烃A、B、C、D的相关信息:
下列给出了四种烃A、B、C、D的相关信息: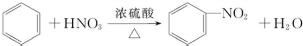 .
. .
.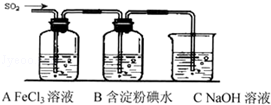 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
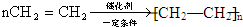 .
.