题目内容
已知有反应:Cu2O+2H+→Cu+Cu2++H2O,则可用来检验氢气还原CuO所得的红色固体中是否含Cu2O的试剂是( )
| A、稀硝酸 | B、稀硫酸 |
| C、盐酸 | D、浓硫酸 |
考点:物质的检验和鉴别的基本方法选择及应用,铜金属及其重要化合物的主要性质
专题:物质检验鉴别题
分析:Cu与非氧化性酸不反应,若含Cu2O,加非氧化性酸得到蓝色溶液,以此鉴别.
解答:
解:氢气还原CuO所得的红色固体中有Cu,可能含Cu2O,由Cu2O+2H+→Cu+Cu2++H2O及Cu与非氧化性酸不反应,则加稀硫酸或稀盐酸若得到蓝色溶液,则证明含Cu2O,
否则不含;而稀硝酸、浓硫酸均具有强氧化性,与Cu反应,则不能检验,
故选BC.
否则不含;而稀硝酸、浓硫酸均具有强氧化性,与Cu反应,则不能检验,
故选BC.
点评:本题考查物质的检验和鉴别,为高频考点,把握信息中的反应及Cu与稀硫酸、盐酸不反应为解答的关键,注意发生的氧化还原反应原理,题目难度不大.

练习册系列答案
相关题目
在下列各溶液中,离子一定能大量共存的是( )
| A、能与铝反应放出氢气的溶液中:K+、Al3+、Cl-、SO42- |
| B、水电离出来的c(H+)=10-12mol/L的溶液 Na+、Cl-、Br-、Ba2+ |
| C、所含溶质为Na2SO4的溶液 K+、CO32-、NO3-、Al3+ |
| D、室温下,pH=1的无色溶液中:Na+、Fe3+、NO3-、SO42- |
化学无处不在,下列与化学有关的说法正确的是( )
| A、液氨汽化时能吸收大量的热,故可用作制冷剂 |
| B、SO2能漂白纸浆等,故可广泛用于食品的漂白 |
| C、味精的主要成分是蛋白质,烧菜时可加入适量 |
| D、氢氟酸可用于雕刻玻璃制品,这是利用酸的通性 |
已知:①相同温度下溶解度:MgCO3:0.02g/100g水,Mg(OH)2:0.0009g/100g水;
②25℃时,亚磷酸(H3PO3,二元酸)的Ka1=3.7×10-2,Ka2=2.9×10-7;草酸(H2C2O4)的Ka1=5.6×10-2,Ka2=5.4×10-5
③相同条件下电离出S2-的能力:FeS>H2S>CuS,以下离子方程式错误的是( )
②25℃时,亚磷酸(H3PO3,二元酸)的Ka1=3.7×10-2,Ka2=2.9×10-7;草酸(H2C2O4)的Ka1=5.6×10-2,Ka2=5.4×10-5
③相同条件下电离出S2-的能力:FeS>H2S>CuS,以下离子方程式错误的是( )
| A、Mg2++2HCO3-+2Ca+4OH-═Mg(OH)2↓+2CaCO3↓+2H2O |
| B、Cu2++H2S═CuS↓+2H+ |
| C、FeS+2H+═H2S↑+Fe2+ |
| D、H2PO3-+C2O42-═HPO32-+HC2O4- |
化学与生产、生活、社会密切相关,下列有关说法中不正确的是( )
| A、合金材料中可能含有非金属元素 |
| B、人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
| C、人体内没有能使纤维素水解成葡萄糖的酶,因此纤维素不能作为人类的营养食物 |
| D、柠檬、桔子等虽然是具有酸味的水果,但属于碱性食物 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1 mol?L-1 Fe(NO3)2溶液:Mg2+、H+、SO42-、Cl- |
| B、0.1 mol?L-1 Ag(NH3)2OH溶液:Na+、H+、Cl-、NO3- |
| C、与金属铝能产生大量H2的溶液:K+、Na+、HCO3-、NO3- |
| D、c(H+)+c(OH-)=2×10-7mol?L-1的溶液:K+、Na+、Br-、Cl- |
下列表述正确的是( )
| A、由水电离出的c(H+)=10-13mol?L-1的溶液中,Na+、NO3-、SO42-、Cl-一定能大量共存 |
| B、与强酸、强碱都能反应的物质种类只有两性氧化物或两性氧氧化物 |
| C、在NaHS溶液中存在的电离有:NaHS=Na++HS-,HS-?H++S2-,H2O?H++OH-,S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH- |
| D、若酸性HA>HB,则等物质的量浓度等体积的NaA和NaB溶液混合后,离子浓度关系为:c(OH-)>c(B-)>c(A-)>c(H+) |
铋(Bi)在医药方面有重要应用,下列关于
Bi和
Bi的说法正确的是( )
209 83 |
210 83 |
| A、两者互为同素异形体 | ||||
B、
| ||||
C、
| ||||
| D、两者分别含有126和127个质子 |
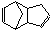 )是一种化学活性很高的烃,存在于煤焦油中.
)是一种化学活性很高的烃,存在于煤焦油中.