题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1 mol?L-1 Fe(NO3)2溶液:Mg2+、H+、SO42-、Cl- |
| B、0.1 mol?L-1 Ag(NH3)2OH溶液:Na+、H+、Cl-、NO3- |
| C、与金属铝能产生大量H2的溶液:K+、Na+、HCO3-、NO3- |
| D、c(H+)+c(OH-)=2×10-7mol?L-1的溶液:K+、Na+、Br-、Cl- |
考点:离子共存问题
专题:电化学专题
分析:A.硝酸根离子在酸性条件下能够氧化亚铁离子;
B.氢离子能够与Ag(NH3)2OH发生反应;
C.与金属铝能产生大量H2的溶液为酸性或者碱性溶液,碳酸氢根离子既能够与氢离子反应,也能够与氢氧根离子反应;
D.c(H+)+c(OH-)=2×10-7mol?L-1的溶液为中性溶液,K+、Na+、Br-、Cl-离子之间不发生反应.
B.氢离子能够与Ag(NH3)2OH发生反应;
C.与金属铝能产生大量H2的溶液为酸性或者碱性溶液,碳酸氢根离子既能够与氢离子反应,也能够与氢氧根离子反应;
D.c(H+)+c(OH-)=2×10-7mol?L-1的溶液为中性溶液,K+、Na+、Br-、Cl-离子之间不发生反应.
解答:
解:A.NO3-在酸性条件下能够氧化NFe2+离子,在溶液中不能大量共存,故A错误;
B.Ag(NH3)2OH能够与氢离子发生反应,在溶液中不能大量共存,故B错误;
C.该溶液为酸性或者碱性溶液,HCO3-既能与氢离子反应,也能与氢氧根离子反应,在溶液中一定不能大量共存,故C错误;
D.K+、Na+、Br-、Cl-之间不反应,无论酸性碱性溶液中都能够大量共存,故D正确;
故选D.
B.Ag(NH3)2OH能够与氢离子发生反应,在溶液中不能大量共存,故B错误;
C.该溶液为酸性或者碱性溶液,HCO3-既能与氢离子反应,也能与氢氧根离子反应,在溶液中一定不能大量共存,故C错误;
D.K+、Na+、Br-、Cl-之间不反应,无论酸性碱性溶液中都能够大量共存,故D正确;
故选D.
点评:本题考查离子共存的正误判断,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”.

练习册系列答案
相关题目
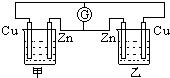 在如图的装置中,甲、乙两烧杯中都盛有相同体积的0.1mol/L的硫酸溶液,下列有关实验的叙述中,错误的是( )
在如图的装置中,甲、乙两烧杯中都盛有相同体积的0.1mol/L的硫酸溶液,下列有关实验的叙述中,错误的是( )| A、电流计G的指针不动 |
| B、通过电流计G的电子流动方向是由下向上 |
| C、甲、乙两装置都不是电解槽 |
| D、甲装置中铜极上有气泡产生,乙装置中,[H+]会减小 |
氨甲环酸和氨甲苯酸是临床上常用的止血药,其结构如图所示:

下列说法错误的是( )

下列说法错误的是( )
| A、氨甲环酸、氨甲苯酸都既能溶于盐酸,又能溶于NaOH溶液 |
| B、氨甲苯酸属于芳香族α-氨基酸的同分异构体和苯丙氨酸互为同系物 |
| C、氨甲环酸、氨甲苯酸都能发生取代、氧化、缩聚、加成等反应 |
| D、氨甲环酸、氨甲苯酸中各有5种不同的氢原子 |
已知有反应:Cu2O+2H+→Cu+Cu2++H2O,则可用来检验氢气还原CuO所得的红色固体中是否含Cu2O的试剂是( )
| A、稀硝酸 | B、稀硫酸 |
| C、盐酸 | D、浓硫酸 |
葡萄糖在人体中进行无氧呼吸产生乳酸,结构简式如下: ,下列有关乳酸的说法不正确的是( )
,下列有关乳酸的说法不正确的是( )
 ,下列有关乳酸的说法不正确的是( )
,下列有关乳酸的说法不正确的是( )| A、乳酸能发生催化氧化、取代反应 |
| B、乳酸和葡萄糖所含官能团相同 |
| C、乳酸能和碳酸氢钠、钠反应放出气体 |
D、乳酸和 互为同分异构体 互为同分异构体 |
用如图实验装置进行相应实验,装置正确且能达到实验目的是( )
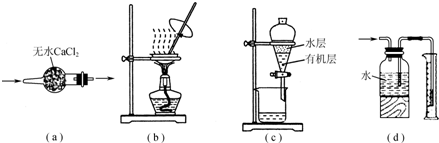

| A、用图a所示装置干燥SO2气体 |
| B、用图b所示装置蒸发CH3COONa溶液得醋酸钠晶体 |
| C、用图c所示装置分离有机层与水层,水层从分液漏斗下口放出 |
| D、用图d所示装置测量氨气的体积 |
下列表示对应化学反应的离子方程式正确的是( )
| A、明矾溶液中滴加过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| B、醋酸溶液与Mg(OH)2反应:Mg(OH)2+2H+═Mg2++2H2O |
| C、小苏打溶液中加足量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| D、SO2通入FeCl3溶液中:SO2+Fe3++2H2O═SO42-+Fe2++4H+ |
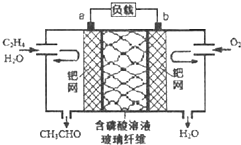 乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:CH2=CH2+O2→2CH3CHO.下列有关说法正确的是( )| A、该电池为可充电电池 |
| B、每有0.1mol O2反应,则迁移H+0.4mol |
| C、正极反应式为:CH2=CH2-2e-+2OH-═CH3CHO+H2O |
| D、电子移动方向:电极a→磷酸溶液→电极b |