题目内容
下列表述正确的是( )
| A、由水电离出的c(H+)=10-13mol?L-1的溶液中,Na+、NO3-、SO42-、Cl-一定能大量共存 |
| B、与强酸、强碱都能反应的物质种类只有两性氧化物或两性氧氧化物 |
| C、在NaHS溶液中存在的电离有:NaHS=Na++HS-,HS-?H++S2-,H2O?H++OH-,S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH- |
| D、若酸性HA>HB,则等物质的量浓度等体积的NaA和NaB溶液混合后,离子浓度关系为:c(OH-)>c(B-)>c(A-)>c(H+) |
考点:电解质在水溶液中的电离,盐类水解的原理,离子共存问题
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:A.由水电离出来的氢离子浓度为10-13mol/L的溶液中,为酸或碱溶液,结合离子反应发生的条件判断;
B.碳酸氢钠与强酸、强碱都能反应,属于盐;
C.S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH- 是离子水解的离子方程式;
D.相同温度下的相同浓度的不同一元酸,酸的酸性越强,则酸的电离程度越大,其阴离子的水解能力越小,据此分析解答.
B.碳酸氢钠与强酸、强碱都能反应,属于盐;
C.S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH- 是离子水解的离子方程式;
D.相同温度下的相同浓度的不同一元酸,酸的酸性越强,则酸的电离程度越大,其阴离子的水解能力越小,据此分析解答.
解答:
解:A.由水电离出来的氢离子浓度为10-13mol/L的溶液中,溶液为酸或碱溶液,Na+、NO3-、SO42-、Cl-一不论是在酸溶液还是碱溶液都不发生反应,所以一定能大量共存,故A正确;
B.碳酸氢钠与强酸、强碱都能反应,属于盐,故B错误;
C.S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH- 是离子水解的离子方程式,故C错误;
D.若酸性HA>HB,则A-水解能力小于B-,等物质的量浓度等体积的NaA和NaB溶液混合后c(B-)<c(A-),故D错误;
故选:A.
B.碳酸氢钠与强酸、强碱都能反应,属于盐,故B错误;
C.S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH- 是离子水解的离子方程式,故C错误;
D.若酸性HA>HB,则A-水解能力小于B-,等物质的量浓度等体积的NaA和NaB溶液混合后c(B-)<c(A-),故D错误;
故选:A.
点评:本题考查了物质在水溶液中的行为,涉及的知识有电解质的电离、盐类的水解、离子的共存,都是高考题中常考查的内容,题目难度中等,把握电解质电离和盐类水解的实质是解题的关键.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
已知有反应:Cu2O+2H+→Cu+Cu2++H2O,则可用来检验氢气还原CuO所得的红色固体中是否含Cu2O的试剂是( )
| A、稀硝酸 | B、稀硫酸 |
| C、盐酸 | D、浓硫酸 |
用如图实验装置进行相应实验,装置正确且能达到实验目的是( )
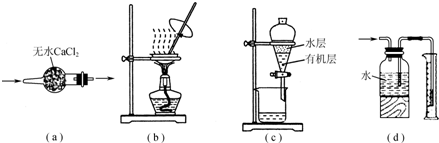

| A、用图a所示装置干燥SO2气体 |
| B、用图b所示装置蒸发CH3COONa溶液得醋酸钠晶体 |
| C、用图c所示装置分离有机层与水层,水层从分液漏斗下口放出 |
| D、用图d所示装置测量氨气的体积 |
化学与生活、社会密切相关.下列说法中正确的是( )
| A、酿酒过程中,葡萄糖可通过水解反应生成酒精 |
| B、利用催化转化装置可以将汽车尾气中的NO和CO转化为无害气体 |
| C、酸性高锰酸钾溶液中加入植物油充分振荡后,溶液紫色不会褪去 |
| D、制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
下列表示对应化学反应的离子方程式正确的是( )
| A、明矾溶液中滴加过量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| B、醋酸溶液与Mg(OH)2反应:Mg(OH)2+2H+═Mg2++2H2O |
| C、小苏打溶液中加足量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| D、SO2通入FeCl3溶液中:SO2+Fe3++2H2O═SO42-+Fe2++4H+ |
以下情况都有气体产生,其中不产生红棕色气体的是( )
| A、加热浓硝酸 |
| B、光照硝酸银 |
| C、加热硝酸钙 |
| D、加热溴化钾和浓硫酸混合物 |