题目内容
8.已知下列两个热化学方程式:H2(g)+$\frac{1}{2}$O2(g)═H2O(l);△H=-285kJ•mol-1
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l);△H=-2220.0kJ•mol-1
又知:H2O(g)═H2O(l);△H=-44.0kJ•mol-1,写出丙烷燃烧生成二氧化碳气体和水蒸气的热化学方程式:C3H8(g)+5O2(g)═3CO2(g)+4H2O(g)△H=-2044.0kJ•mol-1.
分析 ①C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220.0kJ•mol-1,
②H2O(g)═H2O(l)△H=-44.0kJ•mol-1,
由盖斯定律可知,①-②×4可得C3H8(g)+5O2(g)═3CO2(g)+4H2O(g),以此来解答.
解答 解:由①C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220.0kJ•mol-1,
②H2O(g)═H2O(l)△H=-44.0kJ•mol-1,
结合盖斯定律可知,①-②×4可得C3H8(g)+5O2(g)═3CO2(g)+4H2O(g),则△H=(-2220.0kJ•mol-1)-(-44.0kJ•mol-1)×4=-2044.0kJ•mol-1,
所以丙烷燃烧生成二氧化碳气体和水蒸气的热化学方程式为C3H8(g)+5O2(g)═3CO2(g)+4H2O(g)△H=-2044.0kJ•mol-1,
故答案为:C3H8(g)+5O2(g)═3CO2(g)+4H2O(g)△H=-2044.0kJ•mol-1.
点评 本题考查热化学反应方程式的书写,为高频考点,把握盖斯定律的应用、物质的状态及热化学反应方程式的书写为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
8. 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
Ⅰ.实验原理:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
Ⅱ.实验设计:
(1)【方案一】测量气体产物:在相同温度下,利用如图装置,测定不同浓度H2C2O4溶液与KMnO4反应产生相同体积CO2所需的时间(忽略CO2溶解性的影响).如图方框中应选择①②④⑤⑥(填编号)仪器组装量气装置,限选以下仪器:①广口瓶、②双孔塞、③水槽、④橡胶管、⑤导管、⑥量筒.
(2)【方案二】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间.拟定实验数据:表中①、②处的数据分别是5.0、25.
Ⅲ.讨论与交流:
(3)实验室常用KMnO4标准溶液滴定某浓度草酸.KMnO4溶液置于酸式滴定管(填“酸式”或“碱式”)中,判断到达滴定终点的现象是当滴入最后一滴KMnO4溶液时,溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.Ⅰ.实验原理:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
Ⅱ.实验设计:
(1)【方案一】测量气体产物:在相同温度下,利用如图装置,测定不同浓度H2C2O4溶液与KMnO4反应产生相同体积CO2所需的时间(忽略CO2溶解性的影响).如图方框中应选择①②④⑤⑥(填编号)仪器组装量气装置,限选以下仪器:①广口瓶、②双孔塞、③水槽、④橡胶管、⑤导管、⑥量筒.
(2)【方案二】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间.拟定实验数据:表中①、②处的数据分别是5.0、25.
| 实验序号 | 温度/℃ | 各物质的体积/mL | 反应时间 | |||
| H2O | 3mol/L稀硫酸 | 0.1mol/L KMnO4溶液 | 0.6mol/LH2C2O4溶液 | |||
| 1 | 25 | 3.0 | 2.0 | 4.0 | 6.0 | t1 |
| 2 | 25 | ① | 2.0 | 4.0 | 4.0 | t2 |
| 3 | ② | 7.0 | 2.0 | 4.0 | 2.0 | t3 |
(3)实验室常用KMnO4标准溶液滴定某浓度草酸.KMnO4溶液置于酸式滴定管(填“酸式”或“碱式”)中,判断到达滴定终点的现象是当滴入最后一滴KMnO4溶液时,溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
9.已知高炉炼铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.下列对该反应的叙述不正确的是( )
| A. | CO是还原剂 | B. | Fe2O3被还原 | C. | 氧化产物是CO2 | D. | 属于置换反应 |
6.短周期元素A、B、C的原子序数依次增大,其族序数之和为13,且C的族序数是B的族序数的3倍.下列说法正确的是( )
| A. | 三种元素的原子半径:B最小 | |
| B. | 最高价氧化物对应的水化物:仅B呈碱性 | |
| C. | 常温下,B在A、C的最高价氧化物对应的水化物浓溶液中会发生钝化 | |
| D. | A、B、C的氧化物都是形成酸雨的罪魁祸首 |
13.下列各组有机物不管它们以任何比例混合,只要混合物的物质的量一定,则在完全燃烧时消耗氧气的量恒定不变的是( )
| A. | C3H6和C3H8 | B. | C4H6和C3H8 | C. | C5H12和C6H6 | D. | C3H6和C3H8O |
20.已知CaCO3(s)═CaO(s)+CO2(g)△H=+178.5kJ/mol要使1t CaCO3完全分解,热量由煤炭燃烧提供,至少需要煤炭( )千克(已知煤炭热值为33kJ/g)
| A. | 27 | B. | 54.1 | C. | 100 | D. | 154 |
18.下列说法不正确的是( )
| A. | 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 | |
| B. | 分子式是C3H8O的所有同分异构体共3种 | |
| C. | 用乙醇和浓H2SO4制备乙烯时,不可用水浴加热控制反应的温度 | |
| D. | 迷迭香酸结构如图: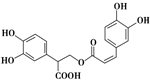 1 mol 迷迭香酸最多能和含6 mol NaOH的水溶液完全反应 1 mol 迷迭香酸最多能和含6 mol NaOH的水溶液完全反应 |