题目内容
20.已知CaCO3(s)═CaO(s)+CO2(g)△H=+178.5kJ/mol要使1t CaCO3完全分解,热量由煤炭燃烧提供,至少需要煤炭( )千克(已知煤炭热值为33kJ/g)| A. | 27 | B. | 54.1 | C. | 100 | D. | 154 |
分析 根据1t CaCO3完全分解吸收的热量等于煤炭燃烧放出的热量来分析解答.
解答 解:CaCO3(s)═CaO(s)+CO2(g)△H=+178.5kJ/mol,所以1t CaCO3完全分解吸收的热量为:$\frac{1{0}^{6}}{1{0}^{2}}$×178.5kJ=1.785×106kJ,所以需要煤$\frac{1.785×1{0}^{6}}{33kJ/g}$×10-3=54.1kg,故选B.
点评 本题考查热化学方程式的意义、热值的定义等,难度不大,注意根据能量守恒分析解答.

练习册系列答案
相关题目
20.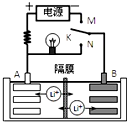 如图是一种可充电的锂离子电池充、放电的工作示意图.该电池的反应式为:
如图是一种可充电的锂离子电池充、放电的工作示意图.该电池的反应式为:
LiMnO2+C6$?_{放电}^{充电}$Li1-xMnO2+LixC6(LixC6表示锂原子嵌入石墨形成的复合材料),下列有关说法正确的是( )
 如图是一种可充电的锂离子电池充、放电的工作示意图.该电池的反应式为:
如图是一种可充电的锂离子电池充、放电的工作示意图.该电池的反应式为:LiMnO2+C6$?_{放电}^{充电}$Li1-xMnO2+LixC6(LixC6表示锂原子嵌入石墨形成的复合材料),下列有关说法正确的是( )
| A. | K与N相接时,A极为负极,该电极反应式为:LixC6-xeˉ=C6+xLi+ | |
| B. | 该电池的比能量与用单质锂作电极的锂电池的比能量相同 | |
| C. | K与M相接时,A极发生氧化反应,LiMnO2-xeˉ=Li1-xMnO2+xLi+ | |
| D. | K与N相接时,Li+由A极区迁移到B极区 |
12.下列关于有机物的说法正确的是( )
| A. | 甲苯和硝基苯均属于芳香烃 | |
| B. | 石油和天然气的主要成分都是碳氢化合物 | |
| C. | CH2=CHBr和CH3COCl 均属于卤代烃 | |
| D. | 分子内含有苯环和羟基的化合物都属于酚类 |
9.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1mol苯乙烯( )中含有的C=C数为4NA )中含有的C=C数为4NA | |
| B. | 在标准状况下,11.2 L己烷含有分子数为0.5NA | |
| C. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| D. | 1mol甲基含10NA个电子 |
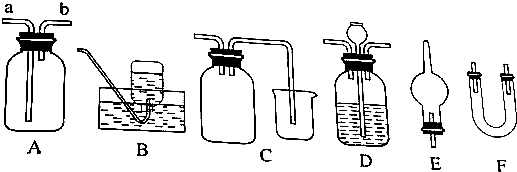
10.制取较纯净的一氯乙烷最好采用的方法是( )
| A. | 乙烷和氯气反应 | B. | 乙烯和氯化氢反应 | ||
| C. | 乙烷通入浓盐酸 | D. | 乙烯和氯气反应 |
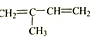 ⑤
⑤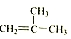
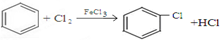 .
. .
. D.
D.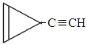 e.
e.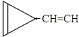 …
… 或
或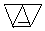 (只需答出一例的结构简式).
(只需答出一例的结构简式).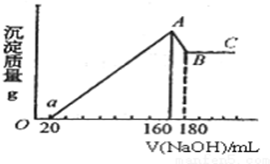 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.
将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.