题目内容
9.已知高炉炼铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.下列对该反应的叙述不正确的是( )| A. | CO是还原剂 | B. | Fe2O3被还原 | C. | 氧化产物是CO2 | D. | 属于置换反应 |
分析 该反应中Fe元素化合价由+3价变为0价、C元素化合价由+2价变为+4价,
A.失电子化合价升高的反应物是还原剂;
B.得电子化合价降低的反应物是氧化剂,氧化剂被还原;
C.还原剂对应的产物是氧化产物,氧化剂对应的产物是还原产物;
D.一种单质和一种化合物反应生成另外的单质和化合物的反应为置换反应.
解答 解:该反应中Fe元素化合价由+3价变为0价、C元素化合价由+2价变为+4价,
A.失电子化合价升高的反应物是还原剂,根据化合价变化知,CO是还原剂,故A正确;
B.得电子化合价降低的反应物是氧化剂,氧化剂被还原,根据化合价变化知,氧化铁是氧化剂,在反应中被还原,故B正确;
C.还原剂对应的产物是氧化产物,氧化剂对应的产物是还原产物,CO是还原剂、氧化铁是氧化剂,所以Fe是还原产物、二氧化碳是氧化产物,故C正确;
D.一种单质和一种化合物反应生成另外的单质和化合物的反应为置换反应,该反应中反应物都是化合物,所以该反应不是置换反应,故D错误;
故选D.
点评 本题考查氧化还原反应,为高频考点,侧重考查基本概念、反应类型判断,明确基本概念内涵是解本题关键,知道常见元素化合价,题目难度不大.

练习册系列答案
相关题目
20.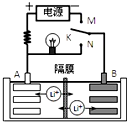 如图是一种可充电的锂离子电池充、放电的工作示意图.该电池的反应式为:
如图是一种可充电的锂离子电池充、放电的工作示意图.该电池的反应式为:
LiMnO2+C6$?_{放电}^{充电}$Li1-xMnO2+LixC6(LixC6表示锂原子嵌入石墨形成的复合材料),下列有关说法正确的是( )
 如图是一种可充电的锂离子电池充、放电的工作示意图.该电池的反应式为:
如图是一种可充电的锂离子电池充、放电的工作示意图.该电池的反应式为:LiMnO2+C6$?_{放电}^{充电}$Li1-xMnO2+LixC6(LixC6表示锂原子嵌入石墨形成的复合材料),下列有关说法正确的是( )
| A. | K与N相接时,A极为负极,该电极反应式为:LixC6-xeˉ=C6+xLi+ | |
| B. | 该电池的比能量与用单质锂作电极的锂电池的比能量相同 | |
| C. | K与M相接时,A极发生氧化反应,LiMnO2-xeˉ=Li1-xMnO2+xLi+ | |
| D. | K与N相接时,Li+由A极区迁移到B极区 |
17.充分燃烧1mol气态烃R,得到标准状况下44.8LCO2和54gH2O,则R是( )
| A. | C2H6 | B. | C2H4 | C. | C2H2 | D. | C4H6 |
14.化合物G(结构如图)是合成抗癌药氨柔比星的中间体.下列说法正确的是( )
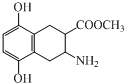

| A. | 该有机物的分子式为C12H14NO4 | |
| B. | 该有机物既可与盐酸反应,又可与NaOH溶液反应 | |
| C. | 该有机物中含有2个手性碳原子 | |
| D. | 1mol该有机物最多只能与1molBr2发生取代反应 |
9.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1mol苯乙烯( )中含有的C=C数为4NA )中含有的C=C数为4NA | |
| B. | 在标准状况下,11.2 L己烷含有分子数为0.5NA | |
| C. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| D. | 1mol甲基含10NA个电子 |