题目内容
2.镁、铝及其化合物在生产生活中具有重要的应用.回答下列问题:(1)工业上冶炼金属镁是采用惰性电极电解熔融MgCl2的方法,此时阴极的电极反应式为:Mg2++2e-=Mg;
(2)除去MgCl2溶液中的Fe2+,常加入少量H2O2,使Fe2+氧化为Fe3+,然后加入少量碱性物质至溶液pH=4,此时c(Fe3+)=4×10-8mol/L[已知Fe(OH)3的Ksp=4×10-38]
(3)工业上冶炼金属铝则是采用惰性电极电解熔融Al2O3的方法,关于为什么不采用电解熔融AlCl3的方法的叙述正确的是C(选择填空):
A.AlCl3是非电解质 B.AlCl3水溶液不导电 C.AlCl3是共价化合物 D.AlCl3熔点太高
(4)用碳棒做电极电解熔融Al2O3时,阳极需要定期更换,其原因是2O2--4e-=O2
C+O2$\frac{\underline{\;高温\;}}{\;}$CO2或2C+O2$\frac{\underline{\;高温\;}}{\;}$2CO(用电极反应式和化学方程式回答);
(5)已知:Al2O3(熔融,l)=2Al(s)+$\frac{3}{2}$O2(g)△H=1600KJ•mol-1工业上利用惰性电极电解熔融Al2O3冶炼铝,每消耗1000kJ电能时,生成27gAl,则电解过程中能量利用率为_80%.
(6)明矾的化学式为KAl(SO4)2•12H2O,它可以作为净水剂,用离子方程式表示其能够净水的原因
Al3++3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Al(OH)3(胶体)+3H+;向明矾溶液中逐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时,溶液的pH>7(填>、<、=);
(7)若在空气中加热固体MgCl2•6H2O,可水解生成Mg(OH)Cl,写出相关的化学方程式MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)Cl+HCl↑+5H2O↑,所以,为了抑制MgCl2•6H2O在加热时水解,可在干燥的HCl气流中加热,可得到无水氯化镁.
分析 (1)电解时阴极是阳离子得到电子发生还原反应,镁离子得到电子生成镁单质;
(2)依据溶液中的溶度积计算铁离子浓度;
(3)氯化铝是共价化合物,熔融固体不能电离出阴阳离子;
(4)碳棒做电极电解熔融氧化铝,阳极上氧离子失电子发生氧化反应生成氧气,氧气和碳反应生成二氧化碳,消耗电极需要定期补充;
(5)根据Al2O3(熔融1)=2Al(s)+$\frac{3}{2}$O2(g)△H=+1600kJ•mol-1,则生成27gAl即1mol时要吸收$\frac{1600}{2}$=800KJ的热量,据此计算;
(6)明矾溶于水发生水解,铝离子水解生成氢氧化铝和硫酸,氢氧化铝具有净水作用,向明矾溶液中逐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时硫酸铝钾和氢氧化钡物质的量之比等于1:2反应生成硫酸钡沉淀、偏铝酸钾和水;
(7)若在空气中加热MgCl2•6H2O,可生成Mg(OH)Cl或MgO,依据原子守恒书写化学方程式;
解答 解:(1)电解熔融MgCl2可得到金属镁,镁离子在阴极放电,电极反应方程式为:Mg2++2e-=Mg,故答案为:Mg2++2e-=Mg;
(2)除去MgCl2溶液中的Fe2+,常加入少量H2O2,使Fe2+氧化为Fe3+,然后加入少量碱性物质至溶液pH=4,c(H+)=10-4mol/L,c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-4}}$=10-10mol/L,此时c(Fe3+)=$\frac{Ksp}{{c}^{3}(O{H}^{-})}$=$\frac{4×1{0}^{-38}}{(1{0}^{-10})^{3}}$=4×10-8,
故答案为:4×10-8;
(3)工业上冶炼金属铝则是采用惰性电极电解熔融Al2O3的方法,不采用电解熔融AlCl3的方法是因为氯化铝是共价化合物,固体熔融会升华,不能得到阴阳离子,不能发生电解反应得到金属铝,氯化铝溶于水完全电离属于电解质,故答案为:C;
(4)碳棒做电极电解熔融氧化铝,阳极上氧离子失电子发生氧化反应生成氧气,电极反应为:2O2--4e-=O2,在冶炼过程中,阳极材料碳被氧气氧化成一氧化碳,反应为C+O2$\frac{\underline{\;高温\;}}{\;}$CO2或2C+O2$\frac{\underline{\;高温\;}}{\;}$2CO,所以需定期地进行更换,
故答案为:2O2--4e-=O2,C+O2$\frac{\underline{\;高温\;}}{\;}$CO2或2C+O2$\frac{\underline{\;高温\;}}{\;}$2CO;
(5)由Al2O3(熔融1)=2Al(s)+$\frac{3}{2}$O2(g)△H=+1600kJ•mol-1,则生成27gAl即1mol时要吸收$\frac{1600}{2}$=800KJ的热量,所以电解过程中能量利用率为$\frac{80}{1000}$×100%=80%,故答案为:80%;
(6)明矾溶于水发生水解,铝离子水解生成氢氧化铝和硫酸,氢氧化铝具有净水作用,即Al3++3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Al(OH)3(胶体)+3H+,向明矾溶液中逐滴加入Ba(OH)2溶液至硫酸根离子刚好沉淀完全时硫酸铝钾和氢氧化钡物质的量之比等于1:2反应生成硫酸钡沉淀、偏铝酸钾和水;偏铝酸钾溶液中水解溶液显碱性,溶液PH>7,
故答案为:Al3++3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Al(OH)3(胶体)+3H+,>;
(7)若在空气中加热MgCl2•6H2O,可生成Mg(OH)Cl或MgO,依据原子守恒书写化学方程式为:MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)Cl+HCl↑+5H2O↑;氯化镁水解显酸性,氯化氢气流中加热防止水解,HCl气流可抑制Mg2+水解;
故答案为:MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)Cl+HCl↑+5H2O↑;HCl;
点评 本题考查了常见化合物性质、电解原理、盐类水解应用、溶度积常数的计算,是考查重点,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 盐酸滴在石灰石上:CO32-+2H+═H2O+CO2↑ | |
| B. | 少量CO2通入氢氧化钠溶液中:2OH-+CO2═CO32-+H2O | |
| C. | NaOH溶液和NaHSO4溶液反应:HSO4-+OH-═SO42+H2O | |
| D. | 稀H2SO4滴在铜片上:Cu+2H+═Cu2++H2↑ |
| A. | 在密闭容器中加入1mol N2和3mol H2,充分反应生成NH3分子数为2NA | |
| B. | 0.1mol-NH2(氨基)中含有的电子数为0.7NA | |
| C. | 30g SiO2中含有的Si-O键数目为2NA | |
| D. | 标准状况下,4.48 L N2所含的共用电子对数0.2NA |
| A. | 该反应的离子方程式为:5Cl2+10 OH-═7Cl-+2ClO-+ClO3-+5H2O | |
| B. | 该反应中,氧化剂与还原剂物质的量之比为5:3 | |
| C. | 上述苛性钾溶液中含有0.3mol的KOH | |
| D. | 反应后生成的ClO-和 ClO3- 两种离子在一定条件下均有氧化性 |
| A. | Na+、NH4+、NO3-、MnO4- | B. | Na+、NO3?、SO42?、I? | ||
| C. | K +、Fe3+、Cl-、Br- | D. | Ba2+、Na+、OH-、CO32- |
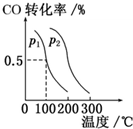 联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.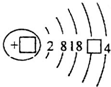 ,请补充完整:
,请补充完整: