题目内容
10. 联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.电解
(1)有效“减碳”的手段之一是节能.下列制氢方法最符合的是C(填字母序号).
A.电解水制氢:2H2O=$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑
B.高温使水分解制氢:2H2O=$\frac{\underline{\;高温\;}}{\;}$2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O$\frac{\underline{\;TiO_{2}\;}}{阳光}$2H2↑+O2↑
D.天然气制氢:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2
(2)用CO2和氢气合成CH3OCH3(甲 醚 )是解决能源危机的研究方向之一.
已知:
CO(g)+2H2(g)═CH3OH(g)△H=Q1 kJ•mol-1
2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=Q2 kJ•mol-1
CO(g)+H2O(g)═CO2(g)+H2(g)△H=Q3 kJ•mol-1
则CO2和氢气合成CH3OCH3(g)的热化学方程式为2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)△H=(2Q1+Q2-2Q3)kJ•mol-1.
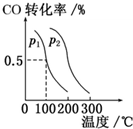
(3)在催化剂和一定温度、压强条件下,CO与H2可反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,则:p1<p2 (填“>”、“<”或“=”),上述反应的△H<0 (填“<”、“>”或“=”)
分析 (1)有效“减碳”的手段之一是节能,利用太阳光催化分解水制氢是最节能的,减少电能、天然气、热能的利用;
(2)利用热化学方程式和盖斯定律计算所需热化学方程式,三式相加得;
(3)根据定一议二原则,相同温度下,同一容器中,增大压强,平衡向正反应方向移动,则CO的转化率增大;
相同压强下,同一容器中,增大温度,CO的转化率减小,平衡向吸热反应方向移动,由此判断.
解答 解:(1)A、消耗电能,不是最节能的方法,故A错误;
B、消耗热能,不是减碳的手段,故B错误;
C、利用太阳光催化分解水制氢是最节能的,故C正确;
D、天然气是非再生能源,且不是最节能的方法,故D错误;故选:C;
(2)利用盖斯定律进行计算,将三个方程式进行形式变换,
2CO(g)+4H2(g)═2CH3OH(g)△H=2Q1 kJ•mol-1
2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=Q2 kJ•mol-1
-2CO(g)-2H2O(g)═-2CO2(g)-2H2(g)△H=-2Q3 kJ•mol-1
三式相加得:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)△H=(2Q1+Q2-2Q3 ) kJ•mol-1,
故答案为:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g)△H=(2Q1+Q2-2Q3 ) kJ•mol-1;
(3)相同温度下,同一容器中,增大压强,平衡向正反应方向移动,则CO的转化率增大,根据图象知,p1小于p2,相同压强下,同一容器中,增大温度,CO的转化率减小,平衡向吸热反应方向移动,所以逆反应为吸热方向,则正反应为放热反应,所以△H<0,
故答案为:<;<.
点评 本题考查盖斯定律的应用,化学平衡移动的影响因素及读图能力,难度不大.

练习册系列答案
相关题目
20.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L H2O含有的分子数为NA | |
| B. | 2L物质的量浓度为0.5mol•/L的MgCl2溶液中,含有Cl- 个数为 NA | |
| C. | 常温下,NA个CO2分子占有的体积为22.4L | |
| D. | 1.06g Na2CO3含有的Na+离子数为0.02 NA |
1.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | agC2H4和C3H6的混合物所含原子总数为$\frac{3a{N}_{A}}{14}$ | |
| B. | 1.00mol/LNaCl溶液100mL,含有6.02×1022个NaCl分子 | |
| C. | 300mL2mol/L蔗糖溶液中所含分子数大于0.6NA | |
| D. | 在常温常压下,2.24LSO2与O2混合气体中所含氧原子数为0.2NA |
18.下列应用或事实没有体现出胶体的性质的是( )
| A. | 在海水与河水交界处,已形成沙洲 | |
| B. | 清晨林间透过缕缕阳光 | |
| C. | 三氯化铁溶液中加入NaOH出现红褐色沉淀 | |
| D. | 向煮熟的豆浆里加入石膏或卤水以生产豆腐 |
5.下列有关物质的性质与应用不相对应的是( )
| A. | 氢氟酸易与SiO2反应,可用于刻蚀玻璃 | |
| B. | Al和Fe2O3能发生铝热反应,可用于焊接钢轨 | |
| C. | NH3具有碱性,可用NH3与灼热的CuO作用制取少量N2 | |
| D. | Fe具有良好的导电性,可用Fe作电解食盐水的阴极材料 |
15.将蔗糖水解,并用新制的氢氧化铜悬浊液检验其水解产物的实验中,要进行的主要操作是( )
①加热
②滴入稀硫酸
③加入新制的氢氧化铜悬浊液
④加入适量的氢氧化钠溶液调节至碱性.
①加热
②滴入稀硫酸
③加入新制的氢氧化铜悬浊液
④加入适量的氢氧化钠溶液调节至碱性.
| A. | ①→②→③→④→① | B. | ②→①→④→③→① | C. | ②→④→①→③→① | D. | ③→④→①→②→① |
19.下列各组有机物中,互为同分异构体的是( )
| A. |  | B. | 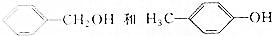 | ||
| C. |  | D. | 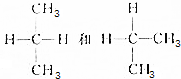 |
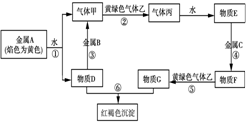 现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、红褐色沉淀H,已知黄绿色气体乙为Cl2,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出),请根据以上信息回答下列问题:
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、红褐色沉淀H,已知黄绿色气体乙为Cl2,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出),请根据以上信息回答下列问题: