题目内容
1.关于如图所示的氢氧燃料电池的说法错误的是( )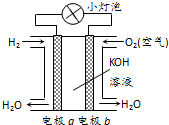
| A. | 电极a是负极 | |
| B. | 电极a上的电极反应为2H2-4e-=4H+ | |
| C. | 外电路中电子由电极a流向电极b | |
| D. | 氢氧燃料电池的优点是高效、对环境友好 |
分析 氢氧燃料电池工作时,是把化学能转变为电能,通入氢气的一极为电源的负极,发生氧化反应,电极反应式为2OH-+H2-2e-=2H2O,通入氧气的一极为原电池的正极,电极反应式为O2+2H2O+4e-=4OH-,电子由负极经外电路流向正极,和电流的流向相反,据此回答.
解答 解:A、氧燃料电池中,H2在负极上a被氧化,O2在正极 b上被还原,所以该电池中电极b是正极,a是负极,故A正确;
B、O2在正极 b上被还原,a是负极,电极反应式为2OH-+H2-2e-=2H2O,故B错误;
C、原电池工作时,电子由负极经外电路流向正极,电子由电极a流向电极b,故C正确;
D、该电池工作时化学能转化为电能,高效,产物是水无污染,对环境友好,故D正确.
故选B.
点评 本题考查原电池的工作原理,题目难度不大,注意正负极的判断及电子流动方向.

练习册系列答案
相关题目
8.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 100mL1mol/LNa2CO3溶液中含有0.1NA个CO32- | |
| B. | 电解精炼铜时,若阴极得到电子数为2NA,则阳极质量减少64g | |
| C. | 1molCl2与过量Fe反应,转移的电子数为2 NA | |
| D. | 标准状况下,11.2L乙醇完全燃烧产生二氧化碳分子数为NA |
12.下列物质所属的类别及其所含官能团的对应关系不正确的是( )
| A. | CH3CH=CH2 烯烃 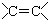 | B. | 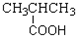 羧酸-COOH 羧酸-COOH | ||
| C. | 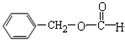 醛类 醛类 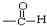 | D. | RCH2OH (R为烃基) 醇类-OH |
6.有a、b、c、d四种金属.将a与b用导线连接起来,浸入电解质溶液中,外电路电流从b流向a.将a、d分别投入到等浓度盐酸中,d比a反应剧烈.将铜浸入b的盐溶液中,无明显变化.如果把铜浸入c的盐溶液中,有金属c析出.据此判断它们的活动性由强到弱的顺序是( )
| A. | dcab | B. | dabc | C. | dbca | D. | dbac |
10.CH3COOH分子中-CH3及-COOH中碳原子的杂化类型分别是( )
| A. | sp3、sp2 | B. | sp3、sp | C. | sp2、sp | D. | sp2、sp3 |
11.下列说法正确的是( )
| A. | P4与CH4的空间构型和键角都相同 | |
| B. | O3与OF2都是V形分子 | |
| C. | SO3和SeO32-的立体构型都是三角锥形 | |
| D. | HOCH2CH(OH)CH2OH与CH3CHClCH2CH3都是手性分子 |

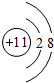 ,A、B、C形成的化合物的电子式为
,A、B、C形成的化合物的电子式为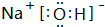 .
.