题目内容
12.下列物质所属的类别及其所含官能团的对应关系不正确的是( )| A. | CH3CH=CH2 烯烃 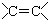 | B. | 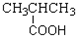 羧酸-COOH 羧酸-COOH | ||
| C. | 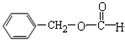 醛类 醛类 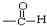 | D. | RCH2OH (R为烃基) 醇类-OH |
分析 A.含碳碳双键;
B.含-COOH;
C.含-COOC-;
D.含-OH.
解答 解:A.丙烯中含碳碳双键,为烯烃,故A正确;
B.2-甲基丙酸中含-COOH,为羧酸,故B正确;
C.甲酸苯甲酯中含-COOC-,为酯类,故C错误;
D.RCH2OH中含-OH,为醇类,故D正确;
故选C.
点评 本题考查有机物的官能团与分类,为高频考点,把握常见有机物中的官能团为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
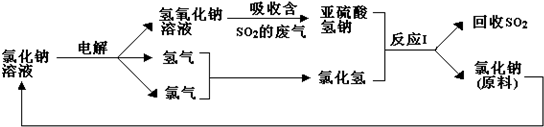
19.硫酸锌和轻质氧化镁在工业生产及食品添加等领域有重要应用.用高镁菱锌矿(主要含ZnCO3、MgCO3、CaCO3以及少量SiO2、Fe2O3、Cu等)进行联合生产.流程如图1:
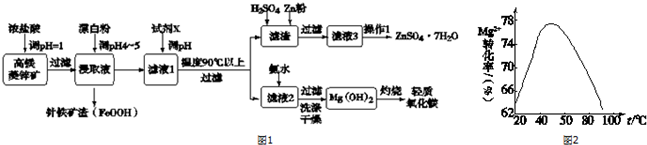
已知:金属离子沉淀的pH
(1)写出浸取过程中产生Fe2+的离子方程式Fe2O3+6H+=2Fe3++3H2O、2Fe3++Cu=2Fe2++Cu2+.
(2)下列说法正确的是acd.
a.用浓盐酸浸取前,将矿石粉碎能够提高浸出速率.
b.试剂X可以选择氨水,pH的范围在8.2~12.4之间.
c.控制温度在90℃以上的目的是为了促进Zn2+的水解.
d.滤渣中加入硫酸后再加入锌粉是为了出去Cu2+.
(3)由Fe2+生成针铁矿渣的离子反应方程式2Fe2++ClO-+3H2O=2FeOOH+Cl-+4H+.
(4)从滤液3中获取ZnSO4•7H2O的操作1是加热浓缩、冷却结晶、过滤、洗涤、干燥.
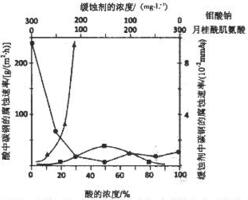
(5)加入氨水制备氢氧化镁的工艺过程要选择适宜条件.图2为反应温度与Mg2+转化率的关系.
①根据图中所示45℃前温度与Mg2+转化率之间的关系,可判断此反应是吸热(填“吸热”或“放热”)反应.
②50℃以上温度升高,Mg2+转化率下降的原因可能是温度过高时,氨水受热分解,浓度降低,Mg2+转化率下降.
③为了获取副产品CaCl2,经常用石灰乳代替氨水来制备氢氧化镁.用平衡移动原理解释石灰乳能够制备氢氧化镁的原因石灰乳中存在Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),Mg2+可以与OH-反应生成更难溶的Mg(OH)2,使得OH-浓度不断下降,平衡右移,最终从Ca(OH)2转化为Mg(OH)2.

已知:金属离子沉淀的pH
| Zn2+ | Mg2+ | Cu2+ | Fe3+ | Fe2+ | |
| 开始沉淀pH | 5.9 | 9.4 | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 8.2 | 12.4 | 6.7 | 3.7 | 9.6 |
(2)下列说法正确的是acd.
a.用浓盐酸浸取前,将矿石粉碎能够提高浸出速率.
b.试剂X可以选择氨水,pH的范围在8.2~12.4之间.
c.控制温度在90℃以上的目的是为了促进Zn2+的水解.
d.滤渣中加入硫酸后再加入锌粉是为了出去Cu2+.
(3)由Fe2+生成针铁矿渣的离子反应方程式2Fe2++ClO-+3H2O=2FeOOH+Cl-+4H+.
(4)从滤液3中获取ZnSO4•7H2O的操作1是加热浓缩、冷却结晶、过滤、洗涤、干燥.
(5)加入氨水制备氢氧化镁的工艺过程要选择适宜条件.图2为反应温度与Mg2+转化率的关系.
①根据图中所示45℃前温度与Mg2+转化率之间的关系,可判断此反应是吸热(填“吸热”或“放热”)反应.
②50℃以上温度升高,Mg2+转化率下降的原因可能是温度过高时,氨水受热分解,浓度降低,Mg2+转化率下降.
③为了获取副产品CaCl2,经常用石灰乳代替氨水来制备氢氧化镁.用平衡移动原理解释石灰乳能够制备氢氧化镁的原因石灰乳中存在Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),Mg2+可以与OH-反应生成更难溶的Mg(OH)2,使得OH-浓度不断下降,平衡右移,最终从Ca(OH)2转化为Mg(OH)2.
20.T℃时,AgCl在水溶液中的沉淀溶解平衡曲线如图所示.在该温度下,下列说法中不正确的是( )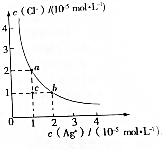

| A. | a点和b点对应的Ksp(AgCl)相等 | |
| B. | Ksp(AgCl)=2×10-10 | |
| C. | 可采取蒸发溶剂的方法使溶液从c点变到b点 | |
| D. | 已知Ksp(AgI)=8.5×10-17,向含KI和KCl的溶液中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$=4.25×10-7 |
4.能说明苯不是单双键交替的事实是( )
| A. | 苯的一氯代物只有一种 | B. | 苯的邻位二氯代物只有一种 | ||
| C. | 苯的间位二氯代物只有一种 | D. | 苯的对位二氯代物只有一种 |
1.关于如图所示的氢氧燃料电池的说法错误的是( )
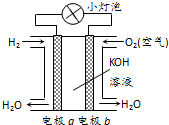

| A. | 电极a是负极 | |
| B. | 电极a上的电极反应为2H2-4e-=4H+ | |
| C. | 外电路中电子由电极a流向电极b | |
| D. | 氢氧燃料电池的优点是高效、对环境友好 |
2.X、Y、Z和M是4种短周期元素,其中X、Y位于同一主族,Y与M、X与Z位于同一周期.X原子最外层电子数是其电子层数的3倍.Z原子的核外电子数比X原子少1.M是同周期中半径最大的元素(除稀有气体元素).下列说法正确的是( )
| A. | Y元素最高价氧化物对应水化物的化学式可表示为H2YO3 | |
| B. | Z和M组成的化合物与盐酸反应可以生成两种盐 | |
| C. | X、Y、Z元素的气态氢化物中,Y的沸点最高 | |
| D. | 四种元素简单离子的半径由大到小依次为Y>X>Z>M |
 .
.
 .
.