题目内容
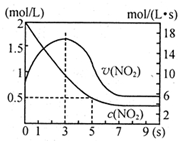 某绝热恒容容器中充入2mol/L NO2,发生反应2NO2?N2O4 △H=-56.9kJ/mol下列分析不正确的是( )
某绝热恒容容器中充入2mol/L NO2,发生反应2NO2?N2O4 △H=-56.9kJ/mol下列分析不正确的是( )| A、5s时NO2的转化率为75% |
| B、0-3s时v(NO2)增大是由于体系温度升高 |
| C、3s时化学反应处于平衡状态 |
| D、9s时再充入N2O4,平衡后K较第一次平衡时大 |
考点:化学平衡建立的过程,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:A、分析图象5s二氧化氮变化浓度=2mol/L-0.5mol/L=1.5mol/L,结合转化率概念计算=
×100%;
B、依据反应是放热反应,在绝热恒容容器中,反应进行热量升高,反应速率增大;
C、3s时二氧化氮反应速率最大,但随时间变化,速率减小,在7s后二氧化氮浓度不变是平衡状态,此时不能说明反应达到平衡状态;
D、9s时反应达到平衡状态,加入N2O4,平衡逆向进行,反应热量降低,平衡向放热分析进行,平衡常数增大.
| 消耗量 |
| 起始量 |
B、依据反应是放热反应,在绝热恒容容器中,反应进行热量升高,反应速率增大;
C、3s时二氧化氮反应速率最大,但随时间变化,速率减小,在7s后二氧化氮浓度不变是平衡状态,此时不能说明反应达到平衡状态;
D、9s时反应达到平衡状态,加入N2O4,平衡逆向进行,反应热量降低,平衡向放热分析进行,平衡常数增大.
解答:
解:A、分析图象5s二氧化氮变化浓度=2mol/L-0.5mol/L=1.5mol/L,结合转化率概念计算=
×100%=
×100%=75%,故A正确;
B、依据反应是放热反应,在绝热恒容容器中,反应进行热量升高,反应速率增大,随反应进行二氧化氮浓度减小,反应为达到平衡,0-3s时v(NO2)增大是由于体系温度升高,故B正确;
C、3s时二氧化氮反应速率最大,但随时间变化,速率减小,在7s后二氧化氮浓度不变是平衡状态,3s此时不是平衡状态,故C错误;
D、9s时反应达到平衡状态,加入N2O4,平衡逆向进行,反应热量降低,平衡向放热分析进行,平衡常数增大,9s时再充入N2O4,平衡后K较第一次平衡时大,故D正确;
故选C.
| 消耗量 |
| 起始量 |
| 1.5mol/L |
| 2mol/L |
B、依据反应是放热反应,在绝热恒容容器中,反应进行热量升高,反应速率增大,随反应进行二氧化氮浓度减小,反应为达到平衡,0-3s时v(NO2)增大是由于体系温度升高,故B正确;
C、3s时二氧化氮反应速率最大,但随时间变化,速率减小,在7s后二氧化氮浓度不变是平衡状态,3s此时不是平衡状态,故C错误;
D、9s时反应达到平衡状态,加入N2O4,平衡逆向进行,反应热量降低,平衡向放热分析进行,平衡常数增大,9s时再充入N2O4,平衡后K较第一次平衡时大,故D正确;
故选C.
点评:本题考查了图象分析判断,反应速率、转化率概念计算分析,平衡状态判断,掌握基础是解题关键,题目难度中等.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
下列说法正确的是( )
| A、甲苯是饱和烃,氯乙烯是不饱和烃 |
| B、石油的裂化产品能使溴水褪色 |
| C、蛋白质在CuSO4溶液中发生盐析 |
| D、油脂在NaOH溶液中水解生成高级脂肪酸和甘油 |
常温下,将0.01mol?L-1 Na2SO3溶液与0.01mol?L-1 KHSO3溶液等体积混合,若忽略混合后溶液的体积的变化,则下列判断正确的量( )
| A、混合后溶液中存在有关系:C(K+)+C(Na+)+C(H+)=C(SO32-)+C(HSO3-)+C(OH-) |
| B、混合后溶液中存在有关系:C(K+)+C(H2SO3)+C(H+)=C(SO32-)+C(OH-) |
| C、混合后溶液中存在有关系:C(SO32-)+C(HSO3-)+C(H2SO3)=0.02 mol?L-1 |
| D、两溶液混合前,Na2SO3溶液中水电离出C(H+)小于KHSO3溶液中水电离出C(H+) |
四种短周期元素在周期表中的位置如图,其中只有M为金属元素.下列说法正确的是( )
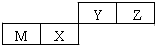
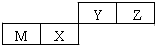
| A、原子半径Z>Y |
| B、X的最简单气态氢化物的热稳定性比Z的小 |
| C、Y的最高价氧化物对应水化物的酸性比X的弱 |
| D、M的最高价氧化物对应水化物不能与NaOH溶液反应 |
人体血液中存在平衡:CO2+H2O?H2CO3
HCO3-,使血液pH保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒.已知pH随c(HCO3-):c(H2CO3)变化关系如下表所示,则下列说法中不正确的是( )
| OH- |
| H- |
| c(HCO3-):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
| A、pH=7的血液中,c(HCO3-)>c(H2CO3) |
| B、人体发生酸中毒时,可静脉滴注一定浓度的NaHCO3溶液解毒 |
| C、常温下将pH=7.40的血液稀释至pH=7时,c(H+)?c(OH-)一定不变 |
| D、c(HCO3-):c(H2CO3)=1时,H2CO3的电离程度小于HCO3-的水解程度 |
下列说法中不正确的是( )
| A、高吸水性树脂属于功能高分子材料 |
| B、SiC、Al2O3的熔点很高,可用作高温结构陶瓷 |
| C、光导纤维、合成纤维和人造纤维都是有机高分子化合物 |
| D、合金拓展了金属材料的使用范围,合金中也可能含有非金属元素 |
下列说法中,正确的是( )
| A、冰熔化时水分子的共价键未发生断裂 |
| B、同族元素的氧化物形成的晶体类型相同 |
| C、分子晶体中,分子间作用力越大,分子越稳定 |
| D、具有高熔沸点的晶体一定是离子晶体或原子晶体 |
 用18.4mol/L的浓H2SO4配制500ml0.5mol/L的稀H2SO4,请按要求填空:
用18.4mol/L的浓H2SO4配制500ml0.5mol/L的稀H2SO4,请按要求填空: