题目内容
下列说法正确的是( )
| A、甲苯是饱和烃,氯乙烯是不饱和烃 |
| B、石油的裂化产品能使溴水褪色 |
| C、蛋白质在CuSO4溶液中发生盐析 |
| D、油脂在NaOH溶液中水解生成高级脂肪酸和甘油 |
考点:有机物的结构和性质,有机化学反应的综合应用
专题:有机反应
分析:A.甲苯中含苯环,氯乙烯中含-Cl;
B.石油的裂化产品主要为烯烃;
C.CuSO4为重金属盐;
D.油脂在NaOH溶液中水解生成高级脂肪酸盐.
B.石油的裂化产品主要为烯烃;
C.CuSO4为重金属盐;
D.油脂在NaOH溶液中水解生成高级脂肪酸盐.
解答:
解:A.甲苯中含苯环,则为不饱和芳香烃;氯乙烯中含-Cl,则属于卤代烃,故A错误;
B.石油的裂化产品主要为烯烃,则能使溴水褪色,故B正确;
C.CuSO4为重金属盐,则蛋白质在CuSO4溶液中发生变性,故C错误;
D.油脂在NaOH溶液中水解生成高级脂肪酸盐和甘油,而在酸性液中水解生成高级脂肪酸和甘油,故D错误;
故选B.
B.石油的裂化产品主要为烯烃,则能使溴水褪色,故B正确;
C.CuSO4为重金属盐,则蛋白质在CuSO4溶液中发生变性,故C错误;
D.油脂在NaOH溶液中水解生成高级脂肪酸盐和甘油,而在酸性液中水解生成高级脂肪酸和甘油,故D错误;
故选B.
点评:本题考查有机物的结构与性质,为高频考点,把握常见有机物的组成、结构、性质为解答的关键,注意相关概念的辨析及石油产品的成分,题目难度不大.

练习册系列答案
相关题目
以下性质的比较可能错误的是( )
| A、离子半径 H->Li+ |
| B、熔点 Al2O3>MgO |
| C、结合质子(H+)的能力 CO32->ClO- |
| D、密度 1-氯戊烷>1-氯己烷 |
现有X、Y、Z三种常见短周期元素,Y、Z为同周期金属元素,且X和Y的某种化合物为淡黄色固体M,Y、Z的最高价氧化物对应的水化物可以反应生成盐N和水.下列说法不正确的是( )
| A、固体M能与水反应生成X单质和一种强碱 |
| B、Z单质的薄片在酒精灯上加热能熔化,但不滴落 |
| C、Y的最高价氧化物对应的水化物和盐N均能抑制水的电离 |
| D、M和N中均含有离子键和共价键 |
有机化合物A转化为B的反应如下,下列说法正确的是( )
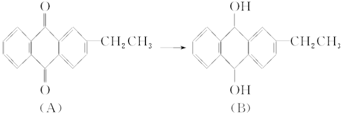

| A、B的分子式为C16H14O2 |
| B、上述转化属于还原反应 |
| C、二者均为芳香烃 |
| D、二者均能发生加成、酯化反应 |
常温时,下列叙述正确的是( )
| A、pH=9的NH4Cl与NH3?H2O混合溶液中c(Cl-)>c(NH4+) |
| B、pH=2.5的可乐中c(H+)是pH=3.5的柠檬水中c(H+)的10倍 |
| C、AgCl在0.1mol/L CaCl2溶液和0.1mol/L NaCl溶液中的溶解度相同 |
| D、1mL 1mol?L-1 Na2CO3溶液加水稀释至100mL,pH和Kw均减小 |
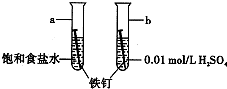 如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )
如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )| A、ab在两处的腐蚀速率a<b |
| B、a、b两处铁钉中的碳均为正极 |
| C、a、b两处铁钉中的铁均失电子被氧化 |
| D、a、b两处的正极反应式均为O2+4e-+4H+═2H2O |
下列说法正确的是( )
| A、0.1mol/L溶液中的(NH4)2SO4溶液中的c(NH4+)<c(SO42-) |
| B、相同温度下,0.6mol/L氨水溶液与0.3 mol/L氨水溶液中c(OH-)之比是2:1 |
| C、向0.1mol/L NaNO3溶液中滴加硝酸使溶液pH=5,此时混合液中的c(Na+)<c(NO3-) |
| D、向醋酸钠溶液中加入适量醋酸,使混合液pH=7,此时混合液中c(Na+)<c(CH3COO-) |
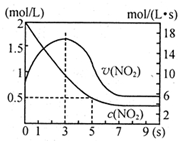 某绝热恒容容器中充入2mol/L NO2,发生反应2NO2?N2O4 △H=-56.9kJ/mol下列分析不正确的是( )
某绝热恒容容器中充入2mol/L NO2,发生反应2NO2?N2O4 △H=-56.9kJ/mol下列分析不正确的是( )| A、5s时NO2的转化率为75% |
| B、0-3s时v(NO2)增大是由于体系温度升高 |
| C、3s时化学反应处于平衡状态 |
| D、9s时再充入N2O4,平衡后K较第一次平衡时大 |
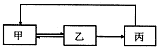 下表中各组物质之间不能通过一步反应实现如图转化的是( )
下表中各组物质之间不能通过一步反应实现如图转化的是( )