题目内容
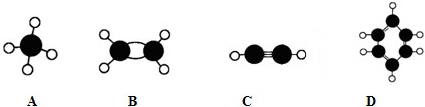
下列说法中,正确的是( )
| A、冰熔化时水分子的共价键未发生断裂 |
| B、同族元素的氧化物形成的晶体类型相同 |
| C、分子晶体中,分子间作用力越大,分子越稳定 |
| D、具有高熔沸点的晶体一定是离子晶体或原子晶体 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A、冰熔化时破坏分子间作用力;
B、H与Na属于同主族元素,二者的氧化物晶体类型不同;
C、分子的稳定性与分子间作用力无关;
D、有的金属晶体的熔沸点也很高.
B、H与Na属于同主族元素,二者的氧化物晶体类型不同;
C、分子的稳定性与分子间作用力无关;
D、有的金属晶体的熔沸点也很高.
解答:
解:A、冰熔化时破坏分子间作用力,水分子的共价键未发生断裂,故A正确;
B、H与Na属于同主族元素,H的氧化物为H2O属于分子晶体,Na氧化物Na2O、Na2O2均为离子晶体,所以二者的氧化物晶体类型不同,故B错误;
C、分子的稳定性与分子间作用力无关,分子的稳定性与分子内的共价键有关,共价键键能越大,分子越稳定,故C错误;
D、具有高熔沸点的晶体不一定是离子晶体或原子晶体,有的金属晶体的熔沸点也很高,如钨熔点在3000℃以上,故D错误;
故选A.
B、H与Na属于同主族元素,H的氧化物为H2O属于分子晶体,Na氧化物Na2O、Na2O2均为离子晶体,所以二者的氧化物晶体类型不同,故B错误;
C、分子的稳定性与分子间作用力无关,分子的稳定性与分子内的共价键有关,共价键键能越大,分子越稳定,故C错误;
D、具有高熔沸点的晶体不一定是离子晶体或原子晶体,有的金属晶体的熔沸点也很高,如钨熔点在3000℃以上,故D错误;
故选A.
点评:本题考查了微粒间的作用力、不同晶体熔沸点的比较等,题目侧重于基础知识的考查,难度不大,注意对基础知识的积累.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
下列有关有机物的说法正确的是( )
| A、甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
| B、米酒变酸的过程涉及了氧化反应 |
| C、乙烯和聚丙烯都能与氢气在一定条件下发生加成反应 |
| D、淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应 |
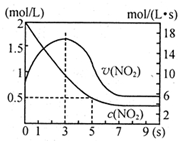 某绝热恒容容器中充入2mol/L NO2,发生反应2NO2?N2O4 △H=-56.9kJ/mol下列分析不正确的是( )
某绝热恒容容器中充入2mol/L NO2,发生反应2NO2?N2O4 △H=-56.9kJ/mol下列分析不正确的是( )| A、5s时NO2的转化率为75% |
| B、0-3s时v(NO2)增大是由于体系温度升高 |
| C、3s时化学反应处于平衡状态 |
| D、9s时再充入N2O4,平衡后K较第一次平衡时大 |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、常温下,9g H2O中含NA个O-H键 |
| B、1mol Fe2+与足量稀硝酸反应,转移3NA个电子 |
| C、常温常压下,22.4L SO2和O2的混合气体中含2NA个氧原子 |
| D、0.1mol?L-1 KAl(SO4)2溶液中含0.2NA个SO42- |
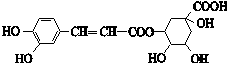 下列有关绿原酸(结构简式如图)的说法不正确的是( )
下列有关绿原酸(结构简式如图)的说法不正确的是( )| A、分子式为C16H18O9 |
| B、1mol绿原酸最多能与8mol NaOH反应 |
| C、1mol绿原酸最多能与4mol H2反应 |
| D、能发生取代反应、消去反应、加成反应和氧化反应 |
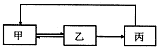 下表中各组物质之间不能通过一步反应实现如图转化的是( )
下表中各组物质之间不能通过一步反应实现如图转化的是( )