题目内容
7.19.2gSO2,其中含氧原子的物质的量为0.6mol,该气体在标准状况下的密度是2.86g/L.分析 根据n=$\frac{m}{M}$计算二氧化硫物质的量,氧原子物质的量为二氧化硫的2倍;标况下气体密度ρ=$\frac{M}{V{\;}_{m}}$.
解答 解:n(SO2)=$\frac{m}{M}$=$\frac{19.2g}{64g.mol{\;}^{-1}}$=0.3mol,
则n(O)=2 n(SO2)=0.6 mol;
标况下ρ(SO2)=$\frac{M}{V{\;}_{m}}$=$\frac{64g/mol}{22.4L/mol}$=2.86g/L,
故答案为:0.6; 2.86g/L.
点评 本题考查物质的量有关计算,难度不大,注意理解掌握标况下气体密度计算.

练习册系列答案
相关题目
14.在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记中的( )
| A. | 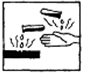 | B. |  | C. |  | D. |  |
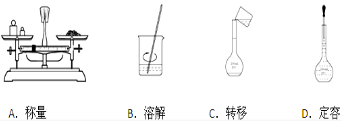
12.下列实验操作错误的是( )
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂不溶于水 |


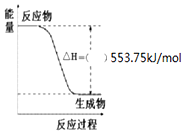 按要求写出298K、101kPa时下列反应的热化学方程式:
按要求写出298K、101kPa时下列反应的热化学方程式: