题目内容
2.CH4、CO2、CO、NaHCO3、Na2CO3等含碳化合物对人类的生产、生活具有重要的意义.(1)已知:甲烷和一氧化碳的燃烧热(△H )分别为-890kJ•moL-1、-283kJ•moL-1.则CH4(g)+2CO2 (g)═4CO(g)+2H2O
(1)△H=+323 kJ•moL-1
(2)一定条件下,在密闭容器中发生的反应为CH4(g)+2CO2 (g)?2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如图Ⅰ.
①据图1可知,该反应的△H=>0(填“>”或“<”).
②刚开始向密闭容器通入2.5mol CH4和4mol CO2,经过5min在A点达到平衡,若容器的体积为2L,则v(CO)=0.2mol/(L•min).平衡常数K=$\frac{8}{3}$,在恒温恒容下,再向该体系中通入1.5mol CH4,2mol CO2、2mol H2 和 2mol CO,化学平衡逆向移动.(填“正向移动”“逆向移动”或“不移动”).
(3)①CO和 H2可以通过反应C(s)+H2O(g)?CO(g)+H2(g)制取.在恒温恒容下,若从反应物开始建立平衡,则下列能判断该反应达到平衡的是AC.
A.体系压强不再变化
B.CO与H2的物质的量之比为1:1
C.混合气体的密度保持不变
D.每消耗1mol H2O(g)的同时生成1mol H2
②在一定条件下,合成气(CO和H2)发生如下两个主要反应:
CO(g)+2H2(g) CH3OH(g)△H=-90.1kJ•moL-1;
2CO(g)+4H2(g) CH30CH3(g)+H20(g)△H=-204.7kJ•moL-1,
仅根据图2可判断该条件下制取甲醇的最佳温度为290℃.

(4)①图3表示的是Na2CO3溶液中各离子浓度的相对大小关系,其中④表示的是HCO3-(填微粒符号)
②常温下,CO32-水解反应的平衡常数即水解常数Kh=2×10 -4 mol•L-1,当溶液中c(CH3-):c(CO32-)=2:1 时,溶液的 pH=10.
分析 (1)根据CH4和CO的燃烧热写出热化学方程式,再据盖斯定律解答;
(2)①根据定一议二,相同压强下,温度高的甲烷平衡转化率高,说明升高温度,有利于正反应,正反应为吸热反应;
②从图可知,A点的平衡,甲烷的转化率为80%,由三段式得反应平衡时的浓度,再计算v(CO)、K;在恒温恒容下,K不变,计算再向该体系中通入1.5mol CH4,2mol CO2、2mol H2 和 2mol CO的Qc,与K比较,可知反应方向;
(3)①根据平衡时正逆反应速率相等,各组分含量保持不变分析;制取甲醇的最佳温度应为CO转化率和CH30CH3产率均较高时;
(4)①碳酸钠溶液中碳酸根离子水解溶液呈碱性,碳酸根离子分步水解;
②CO32-水解反应的平衡常数即水解常数Kh=$\frac{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}{c(C{{O}_{3}}^{2-})}$,当溶c(HCO3-):c(CO32-)=2:1时,根据水解常数计算c(OH-),由根据水的离子积Kw计算c(H+),根据pH=-lgc(H+)计算.
解答 解:(1)CH4和CO的燃烧热分别为809kJ/mol和283kJ/mol,其热化学方程式为:
①CH4(g)+2O2(g)=CO2(g)+2 H2O(l)△H=-809kJ•mol-1
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283kJ•mol-1
据盖斯定律,①-②×4得:CH4(g)+3CO2(g)?4CO(g)+2H2O(g)△H=+323kJ/mol,
故答案为:+323;
(2)①从图可知,相同压强下,温度高的甲烷平衡转化率高,说明升高温度,有利于正反应,正反应为吸热反应,△H>0;
故答案为:>;
②向2L密闭容器通入2.5mol CH4和4mol CO2,5min在A点的平衡,甲烷的转化率为80%,则
CH4(g)+CO2 (g)?2CO(g)+2H2(g)
n始:2.5 4 0 0
n转:2 1 2 2
n平:0.5 3 2 2
则v(CO)=$\frac{2mol÷2L}{5min}$=0.2mol/(L•min);K=$\frac{(2÷2)^{2}×(2÷2)^{2}}{(0.5÷2)×(3÷2)}$=$\frac{8}{3}$;再向该体系中通入1.5mol CH4,2mol CO2、2mol H2 和 2mol CO,此时2mol CH4,5mol CO2、4mol H2 和 4mol CO,浓度商Qc=$\frac{(4÷2)^{2}×(4÷2)^{2}}{(2÷2)(5÷2)}$=6.4>K,所以反应向着逆方向移动;
故答案为:0.2mol/(L•min);$\frac{8}{3}$;逆向移动;
(3)①反应C(s)+H2O(g)?CO(g)+H2(g),恒温恒容条件下,
A.反应气体分子数增大,体系压强增大,不再变化时,反应平衡,故A正确;
B.CO与H2作为产物,生成的物质的量之比始终为为1:1,并不能判断平衡,故B错误;
C.混合气体的质量增大,恒容混合气体的体积不变,密度增大,保持不变时平衡,故C正确;
D.该反应每消耗1mol H2O(g)的同时生成1mol H2,不能说明反应平衡,故D错误;
由图2可知CO转化率和CH30CH3产率均较高时的温度为290℃;
故答案为:AC;290℃;
(4)①Na2CO3溶液中存在水解平衡CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,溶液呈碱性,溶液中离子浓度大小为C(Na+)>C(CO32-)>C(OH-)>C(HCO3-)>C(H+),④为HCO3-;
故答案为:HCO3-;
②c(HCO3-):c(CO32-)=2:1,则Kh=$\frac{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}{c(C{{O}_{3}}^{2-})}$=2c(OH-)=2×10 -4,c(OH-)=$\frac{{K}_{h}}{2}$=$\frac{2×1{0}^{-4}}{2}$=1×10 -4,c(H+)=$\frac{Kw}{c(O{H}^{-})}$=$\frac{1{0}^{-14}}{1{0}^{-4}}$=10-10,所以pH=-lg10-10=10;
故答案为:10.
点评 本题考查盖斯定律、化学平衡状态的判断、化学平衡的有关计算、离子浓度大小比较、盐类水解计算等,题目难度较大,综合考查学生分析问题、解决问题的能力,注重能力的考查.

 请完成下列问题
请完成下列问题(1)已知红磷比白磷稳定,则反应
P4(白磷,s)+5O2(g)═2P2O5(s)△H1;
4P(红磷,s)+5O2(g)═2P2O5(s)△H2;
△H1和△H2的关系是△H1<△H2(填“>”、“<”)
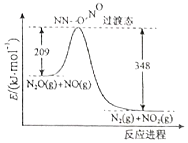
(2)由N2O和NO反应生成1mol N2和NO2的能量变化如图所示,请写出该反应的热化学方程式N2O(g)+NO(g)=N2(g)+NO2(g)△H=-139kJ•moL-1
(3)在298K、101kPa时,已知:
①2H2O(g)═O2(g)+2H2(g)△H1;
②Cl2(g)+H2(g)═2HCl(g)△H2;
③2Cl2(g)+2H2O(g)═4HCl(g)+O2(g)△H3,
则△H3与△H1和△H2之间的关系正确的是A.
A.△H3=△H1+2△H2B.△H3=△H1+△H2
C.△H3=△H1-2△H2D.△H3=△H1-△H2
(4)已知H2(g)+Br2(g)═2HBr(g)△H=-72kJ?mol-1,相关键能数据如表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
| A. | 常温常压下,32 g O3含有的氧原子数目为2NA | |
| B. | 5.6 g的Fe在足量Cl2中完全燃烧转移电子数为0.2NA | |
| C. | 0.1 mol•L-1 Na2SO4溶液含有的钠离子数目为0.2NA | |
| D. | 标准状况下,22.4 L苯含有的碳原子数目为6NA |
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
已知:K300°C>K350°C,则该反应是放热反应.
(2)图中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是bc.
a.v (NO2)=2v (O2) b.容器内压强保持不变
c.v逆(NO)=2v正 (O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
HNO2是一种弱酸,部分弱酸的电离平衡常数如下表:
| 弱酸 | HNO2 | HClO | H2CO3 | H2SO3 |
| 电离平衡常数 (25℃) | Ki=5.1×10-4 | Ki=2.98×10-8 | $\begin{array}{l}{K_{i1}}=4.3×{10^{-7}}\\{K_{i2}}=5.6×{10^{-11}}\end{array}$ | $\begin{array}{l}{K_{i1}}=1.54×{10^{-2}}\\{K_{i2}}=1.02×{10^{-7}}\end{array}$ |
(6)下列离子方程式正确的是BD
A.2ClO-+H2O+CO2→2HClO+CO32-
B.2HNO2+CO32-→2NO2-+H2O+CO2↑
C.H2SO3+CO32-→CO2+H2O+SO32-
D.Cl2+H2O+2CO32-→2HCO3-+Cl-+ClO-
(7)常温下,pH=3的HNO2溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(NO2-)>c(Na+)>c(H+)>c(OH-).
| 甲 | 乙 | 丙 | |
| 容积 | 1L | 1L | 0.5L |
| 起始加入物质 | X:2mol,Y:1mol | Z:2mol | X:0.5mol,Y:0.25mol |
| 平衡时 | c(Z)=1.2mol•L-1 | c(Z)=1.2mol•L-1 |
| A. | T℃时该反应的平衡常数K为3.75 | |
| B. | 平衡时,X转化率:甲<丙 | |
| C. | 若乙是绝热容器,则平衡时,c(Z)>1.2mol•L-1 | |
| D. | 前2min内,丙容器中用X表示的平均反应速率v(X)=0.6mol•L-1 |
②Fe(s)+H2O(g)?FeO(s)+H2(g)?K2
③H2(g)+CO2(g)?H2O(g)+CO(g)?K3
又已知在不同的温度下,K1、K2数值如表:
| 温度℃ | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
(2)反应②的平衡常数表达式为K=$\frac{[H{\;}_{2}]}{[H{\;}_{2}O]}$,此反应在恒温恒容的密闭装置中进行,能充分说明此反应已达到平衡的标志是AB.
A.气体的平均相对分子质量不再改变 B.气体的总质量不再改变
C.气体的总分子数不再改变 D.容器内压强不随时间变化而变化
(3)若900℃时进行反应 ③,其平衡常数K3为1.5(求具体数值),焓变△H>0(填“>”、“<”、“=”).若已知该反应仅在高温时自发进行,则△S>0(填“>”、“<”、“=”).
(4)若500℃时进行反应 ③,在某时刻时C(H2)=C(CO2)=C(H2O)=C(CO),则此时否(填“是”、“否”)达到平衡状态;若没有达到平衡状态,则此时该反应正在向逆(填“正”、“逆”)方向进行,理由为:浓度商=$\frac{[CO]•[H{\;}_{2}O]}{[H{\;}_{2}]•[CO{\;}_{2}]}$=1>K3,所以此时平衡向逆反应方向移动.
 Ⅰ.某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
Ⅰ.某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步: