题目内容
15.可逆反应2NO2?2NO+O2在恒容密闭容器中进行,下列情况达到平衡状态的是( )①单位时间内生成n mol O2的同时生成2n mol NO2
②混合气体的平均相对分子质量不再改变
③NO2、NO、O2的反应速率之比为2:2:1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变.
| A. | ①②④ | B. | ②③⑤ | C. | ①②⑤ | D. | ①②④⑤ |
分析 反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断.
解答 解:①单位时间内生成a mol O2的同时生成2a mol NO2,生成amol氧气,会消耗2amol二氧化氮,说明了正逆反应速率相等,达到了平衡状态,故①正确;
②混合气体的平均相对分子质量不再改变的状态,反应方程式两边完全的物质的量不同,气体的质量固定,所以平均相对分子质量不再改变,说明达到了平衡状态,故②正确;
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态,各组分的浓度大小关系,不能说明各组分的浓度是否变化,正逆反应速率是否相等,故③错误;
④混合气体的颜色不再改变,说明二氧化氮的浓度不再变化,达到了平衡状态,故④正确;
⑤混合气体的密度不再改变的状态,由于反应两边都是气体,容器的体积不变,所以反应中密度始终不变,即密度不能作为判断化学平衡的依据,故⑤错误;
所以正确的有①②④,
故选A.
点评 本题考查化学平衡状态的判断,注意分析时要从化学方程式的反应特征判断,平衡状态的本质时正逆反应速率相等.

练习册系列答案
相关题目
5.下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | A2+与D2-的核外电子数相等 | |
| B. | 氢化物的稳定性为H2E<H2D | |
| C. | B与E形成的化合物既能溶于盐酸又可溶于氢氧化钠溶液 | |
| D. | 最高价氧化物对应水化物碱性:B比A的强 |
6.已知:①H+(aq)+OH-(aq)═H2O(l);△H1;②2SO2(g)+O2(g)?2SO3(g);△H2.其他条件不变时,改变反应物的量,则下列判断正确的是( )
| A. | △H1,△H2都不变 | B. | △H1,△H2都增大 | C. | △H1,△H2都减小 | D. | 不能确定 |
10.表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ):
根据上述数据回答下列问题:
(1)下列物质本身具有的能量最低的是A.
A.H2B.Cl2 C.Br2 D.I2
(2)相同条件下,X2 (X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是Cl2.
(3)已知拆开1mol H-H键、1mol N-H键、1molN≡N 键分别需要吸收的能量为436kJ、391k J、946k J.则由氢气和氮气反应生成1mol NH3需要放出(填“放出”或“吸收”)92 k J的热量.
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
(1)下列物质本身具有的能量最低的是A.
A.H2B.Cl2 C.Br2 D.I2
(2)相同条件下,X2 (X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是Cl2.
(3)已知拆开1mol H-H键、1mol N-H键、1molN≡N 键分别需要吸收的能量为436kJ、391k J、946k J.则由氢气和氮气反应生成1mol NH3需要放出(填“放出”或“吸收”)92 k J的热量.
20.从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O.
(1)为了加快正反应速率,可以采取的措施有ABC(填序号,下同).
A.使用催化剂 B适当提高氧气的浓度
C.适当提高反应的温度 D.适当降低反应的温度
(2)如图能正确表示该反应中能量变化的是A.
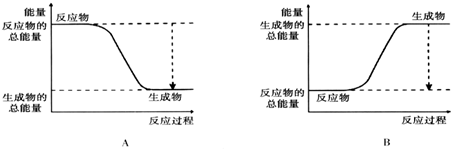
(3)从断键和成键的角度分析上述反应中能量的变化.
请填写下表:
(4)现有如下两个反应:A:NaOH+HCl=NaCl+H2O;B:Fe+2Fe3+=3Fe2+,根据两反应的本质,B能设计成为原电池(填A或B),请画出该原电池装置图.

(1)为了加快正反应速率,可以采取的措施有ABC(填序号,下同).
A.使用催化剂 B适当提高氧气的浓度
C.适当提高反应的温度 D.适当降低反应的温度
(2)如图能正确表示该反应中能量变化的是A.

(3)从断键和成键的角度分析上述反应中能量的变化.
| 化学键 | H-H | O=O | H-O |
| 键能kJ/mol | 436 | 496 | 463 |
| 化学键 | 填“吸收”或“放出”能量 | 能量变化(kJ) | |
| 拆开化学键 | 2molH2中的化学键 | ①吸收热量 | ④1368 |
| 1molO2中的化学键 | |||
| 形成化学键 | 4molH-O键 | ②放出热量 | ⑤1852 |
| 总能量变化 | ③放出热量 | ⑥484 | |

7.下列说法中,不正确的是( )
| A. | 乙醇与金属钠反应时,是乙醇分子中羟基中的O-H键断裂 | |
| B. | 检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水 | |
| C. | 禁止用工业酒精配制饮用酒和调味用的料酒 | |
| D. | 溴乙烷、TNT、丙三醇都是无色溶于水的有机化合物 |
4.设NA为阿佛加德罗常数的值,下列叙述正确的是( )
| A. | 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA | |
| B. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| C. | 4℃时,18g 2H216O中含有共用电子对数为2NA | |
| D. | 常温下,4gCH4含有NA 个C-H共价键 |
5.有A、B、C、D、E五种短周期元素,其元素特征信息如下表.回答下列问题:
(1)写出下列元素的符号:B:O,E:Cl;
(2)写出C与B 形成的两种离子化合物的化学式Na2O;Na2O2.
(3)写出B与A 形成的两种化合物的电子式 ;
;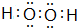 .
.
(4)含B、C、F 三种元素的化合物有Na2SO4、Na2SO3(请填写具体的化学式,至少2种).
(5)D单质和C的最高价氧化物对应水化物水溶液反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(6)FB2和E元素的单质在水溶液中反应的化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4.
(7)D的单质和氧化铁反应可用于野外焊接钢轨,该反应属于放热 (填“吸热”或“放热”)反应,写出反应的化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
| 元素编号 | 元素特征信息 |
| A | 是原子半径最小的元素 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 是短周期元素中原子半径最大的主族元素. |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
| F | 原子有三个电子层,且最外层电子数是最内层电子数的3倍, |
(2)写出C与B 形成的两种离子化合物的化学式Na2O;Na2O2.
(3)写出B与A 形成的两种化合物的电子式
 ;
;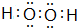 .
.(4)含B、C、F 三种元素的化合物有Na2SO4、Na2SO3(请填写具体的化学式,至少2种).
(5)D单质和C的最高价氧化物对应水化物水溶液反应的离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑.
(6)FB2和E元素的单质在水溶液中反应的化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4.
(7)D的单质和氧化铁反应可用于野外焊接钢轨,该反应属于放热 (填“吸热”或“放热”)反应,写出反应的化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.