��Ŀ����
3����ҵ�ϳɰ���Ӧ��N2+3H2?2NH3��һ�����ȵĿ��淴Ӧ����Ӧ�����Ǹ��¡���ѹ��������Ҫ���ʵĴ�������֪�γ�1mol H-H����1mol N-H����1mol N��N���ų������ֱ�Ϊ436kJ��391kJ��946kJ������1����1mol N2��ȫ��Ӧ����NH3�ɷų�������ա��ų���������92kJ��
��2�������1mol N2��3mol H2��ϣ�ʹ���ַ�Ӧ���ų���������С��������ֵ����ԭ���Ǻϳɰ��ǿ��淴Ӧ����Ӧ�ﲻ����ȫת����
��3��ʵ����ģ�ҵ�ϳɰ�ʱ�����ݻ�Ϊ2L���ܱ������ڣ���Ӧ����10min������10mol NH3������N2��ʾ�Ļ�ѧ��Ӧ����Ϊ0.25mol/��L•min����
��4��һ�������£����ϳɰ��ķ�Ӧ�ﵽ��ѧƽ��ʱ������˵����ȷ����acf��
a������Ӧ���ʺ��淴Ӧ�������
b������Ӧ��������淴Ӧ����Ϊ0
c��N2��ת���ʴﵽ���ֵ
d��N2��H2��Ũ�����
e��N2��H2��NH3������������
f����Ӧ�ﵽ�����
��5�����ĸ���ͬ�����У���ͬ�����½��кϳɰ���Ӧ����������ͬʱ���ڲⶨ�Ľ�����жϸ÷�Ӧ�������ɴ�С��˳����A���ñ����д����
A��V��NH3��=0.5mol•L-1-•min-1 B��V��H2��=0.3mol•L-1-•min-1
C��V��N2��=0.2mol•L-1-•min-1���� ���� D��V��H2��=0.01mol•L-1-•s-1��
���� ��1����H=��Ӧ����ܺ�-��������ܺͣ�
��2���ϳɰ��ǿ��淴Ӧ����Ӧ�ﲻ����ȫת����
��3��v��NH3��=$\frac{\frac{��n}{V}}{��t}$��$\frac{v��{N}_{2}��}{v��N{H}_{3}��}$=$\frac{1}{2}$���ݴ����㣻
��4����ѧƽ��״̬�����淴Ӧ������ȣ������Ũ�ȱ��ֲ����״̬����Ӧ�ﵽ����ȣ��ݴ˷�����
��5��ͬһ��ѧ��Ӧ�У�ͬһʱ����ڣ������ʵķ�Ӧ����֮�ȵ����������֮�ȣ��ȰѲ�ͬ���ʵķ�Ӧ���ʻ����ͬһ���ʵķ�Ӧ���ʽ��бȽϣ��Ӷ�ȷ��ѡ�ע�ⵥλ�Ƿ���ͬ��
��� �⣺��1����H=��Ӧ����ܺ�-��������ܺͣ���ӦN2+3H2?2NH3�С�H=��946+3��436-6��391��kJ/mol=-92kJ/mol����������Ӧ���ȣ�
�ʴ�Ϊ���ų���92��
��2���ϳɰ��ǿ��淴Ӧ����Ӧ�ﲻ����ȫת����
�ʴ�Ϊ���ϳɰ��ǿ��淴Ӧ����Ӧ�ﲻ����ȫת����
��3��v��NH3��=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{10mol}{2L}}{10min}$=0.5mol/��L•min����$\frac{v��{N}_{2}��}{v��N{H}_{3}��}$=$\frac{1}{2}$������v��N2��=0.25mol/��L•min����
�ʴ�Ϊ��0.25mol/��L•min����
��4��a������Ӧ���ʺ��淴Ӧ������ȣ�˵����Ӧ�ﵽƽ��״̬����ȷ��
b������Ӧ��������淴Ӧ����Ϊ0����ָ��Ӧ��ʼʱ��״̬����Ӧû�дﵽƽ��״̬������
c��N2��ת���ʴﵽ���ֵ��˵����Ӧ�ﵽƽ��״̬����ȷ��
d��N2��H2��Ũ����ȣ���Ӧ��һ���ﵽƽ��״̬������
e��N2��H2��NH3�����������ȣ���ƽ��״̬�أ�����
f����Ӧ�ﵽ����ȣ�˵����Ӧ�ﵽƽ��״̬����ȷ��
�ʴ�Ϊ��acf��
��5����ӦΪN2��g��+3H2��g��?2NH3��g�����������ķ�Ӧ����Ϊ�������жϣ�
A��V��NH3��=0.5mol/��L•min������Ӧ����֮�ȵ����������֮�ȣ����Ԧͣ�H2��=0.75mol/��L•min����
B���ͣ�H2��=0.3mol/��L•min����
C���ͣ�N2��=0.2mol/��L•min������Ӧ����֮�ȵ����������֮�ȣ����Ԧͣ�H2��=0.6mol/��L•min����
D���ͣ�H2��=0.01mol/��L•S��=0.6mol/��L•min����
���Է�Ӧ����������A��
��ѡA��
���� ���⿼���˾ݼ��ܼ����ʱ䡢���淴Ӧ���ʱ䡢��ѧ��Ӧ���ʵļ��㼰��С�Ƚϡ���ѧƽ��״̬���жϣ���Ŀ�ѶȲ���

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�| A�� | ��Һ����������ǿ | B�� | ͭƬ���ܽ� | ||
| C�� | ��Һ��H+��пƬ�������ƶ� | D�� | пƬ�Ǹ����������� |
| A�� | Be��OH��2�������������� | |||||
| B�� | ��۲�����ˮ��������CS2�� | |||||
| C�� | O3��SO2�Ľṹ������ | |||||
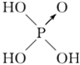
| D�� | ��ͼ֪���ԣ�H3PO4��HClO����ΪH3PO4�ķ��ǻ���ԭ�������ڴ�����ķ��ǻ���ԭ����
|
| A�� | DԪ�ش���Ԫ�����ڱ��е������ڢ�A�� | |
| B�� | ����Ԫ�ص�ԭ�Ӱ뾶��A��B��D��C | |
| C�� | B��D������������������� | |
| D�� | һ�������£�B�������û���D���ʣ�C�������û���A���� |
| A�� | ±��Ԫ���ǵ��͵ķǽ���Ԫ�أ���˲����������ǽ���Ԫ�ط�Ӧ | |
| B�� | �����Ԫ�ص���Խ���ã����۵�ͷе��Խ�� | |
| C�� | ±��Ԫ�ص��ʶ��ܺ�������Ӧ������̬�⻯����ȶ����浥�������Ե���ǿ����ǿ | |
| D�� | ±��Ԫ�ص��ʶ�����ˮ���ҷ�Ӧ |
| A�� | H2O��D2O����ͬ�������� | |
| B�� | 1H��D����ͬλ�� | |
| C�� | 뮣�D��ԭ�Ӻ�����1������ | |
| D�� | 1H218O��D216O����Է���������ͬ |
�ٵ�λʱ��������n mol O2��ͬʱ����2n mol NO2
�ڻ�������ƽ����Է����������ٸı�
��NO2��NO��O2�ķ�Ӧ����֮��Ϊ2��2��1
�ܻ���������ɫ���ٸı�
�ݻ��������ܶȲ��ٸı䣮
| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �٢ڢ� | D�� | �٢ڢܢ� |
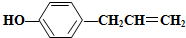 ��������������ȷ���ǣ�������
��������������ȷ���ǣ�������| A�� | 1 mol������������4 mol����������Ӧ | |
| B�� | 1 mol������������3 mol��ˮ������Ӧ | |
| C�� | �����ۿ����Ȼ�����Һ��Ӧ��ʹ��Һ����ɫ | |
| D�� | ��������NaHCO3��Һ��Ӧ����CO2 |
| ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
| ���������mL�� | 50 | 120 | 232 | 290 | 310 |
��2����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����Ϊ0.1mol/��L•min����
��3�������Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ��������������������зֱ����������������Һ��
A������ˮ B��NaCl��Һ C��Na2CO3��Һ D��CuSO4��Һ
����Ϊ���е���AB�����ţ���