题目内容
13.下列元素中,原子M层电子数与K层数相同的有( )| A. | F | B. | Mg | C. | Al | D. | Si |
分析 某元素M层与K层的电子数相同,说明该元素的M层的电子数是2,其核外电子数=2+8+2=12,原子核外电子数=原子序数,据此判断元素.
解答 解:某元素原子核外M层与K层的电子数相同,说明该元素的M层的电子数是2,其核外电子数=2+8+2=12,原子核外电子数=原子序数=12,所以该元素是Mg元素,故选B.
点评 本题考查了元素判断,明确原子结构、原子核外电子排布即可解答,题目难度不大.

练习册系列答案
相关题目
10.下列金属冶炼的反应原理,错误的是( )
| A. | 2NaCl(熔融)$\stackrel{通电}{→}$ 2Na+Cl2↑ | B. | MgO+H2$\stackrel{△}{→}$Mg+H2O | ||
| C. | Fe3O4+4CO3$\stackrel{高温}{→}$Fe+4CO2 | D. | 2HgO 2$\stackrel{△}{→}$Hg+O2↑ |
1.下列排列顺序不正确的是( )
| A. | 非金属性:F>Cl>Br | B. | 原子半径:Na>S>F | ||
| C. | 酸性:H2SO4>H3PO4>H4SiO4 | D. | 热稳定性:H2O>HF>H2S |
18.下列物质性质变化规律正确的是( )
| A. | HI、HBr、HCl、HF的沸点依次降低 | B. | O、F、H的原子半径依次减小 | ||
| C. | 干冰、钠、冰的熔点依次降低 | D. | 金属Na、Mg、Al的硬度依次降低 |
2.下列说法都正确的是( )
①生活中使用频率很高的一元纸币将逐步被硬币替代,硬币是合金
②江河入海口三角洲的形成通常与胶体的性质有关
③“钡餐”中使用的硫酸钡是弱电解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和H2O2,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物.
①生活中使用频率很高的一元纸币将逐步被硬币替代,硬币是合金
②江河入海口三角洲的形成通常与胶体的性质有关
③“钡餐”中使用的硫酸钡是弱电解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和H2O2,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物.
| A. | ①②③④ | B. | ①②④⑥ | C. | ①②⑤⑥ | D. | ③④⑤⑥ |
3.下列各组离子在溶液中能大量共存的是( )
| A. | Fe3+、Cl-、NO3- | B. | K+、HCO3-、OH- | C. | Na+、HCO3-、H+ | D. | NH4+、H+、SO32- |
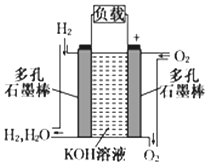 被誉为改变未来世界十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如下图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
被誉为改变未来世界十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如下图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题: ;
;