题目内容
5. 磷元素的单质及其化合物在生产和生活中有着广泛的应用.
磷元素的单质及其化合物在生产和生活中有着广泛的应用.I.用磷矿石在高温下制备白磷(P4)的化学方程式为:2Ca3(PO4)2(s)+10C(s)→P4(g)+6CaO(s)+10CO(g)
(1)反应中破坏的化学键有abc.
a.离子键 b.极性共价键 c.非极性共价键
(2)白磷肯定不具有的性质是c(单项选择).
a.与强碱发生自身氧化还原反应 b.易溶于CS2
c.点燃时和氢气化合生成PH3 d.易自燃
(3)P4分子呈正四面体结构,分子中有6个P-P键,键角为600.
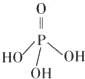
Ⅱ.磷酸分子结构式见图.三聚磷酸可视为三个磷酸分子之间脱去两个水分子产物,其结构式为
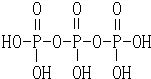 .
.| 电离常数(25℃) |
| HF:Ki=3.6×10 -4 |
| H3PO4:Ki1=7.5×10 -3, Ki2=6.2×10 -8,Ki3=2.2×10 -13 |
(6)NH3比PH3更易液化,原因可能是c(单项选择).
a.H-N键键能大于H-P键键能
b.NH3分子间范德华力大于PH3分子间范德华力
c.其它原因.
分析 I.(1)Ca3(PO4)2含离子键、极性共价键,C含非极性共价键;
(2)白磷为非极性分子,着火点低,不能在空气中燃烧,可与碱液反应;
(3)P4分子呈正四面体结构,含6个P-O键,每个面为等边三角形;
Ⅱ.(4)三聚磷酸可视为三个磷酸分子之间脱去两个水分子产物,则分子中含3个P,4个-OH;
(5)少量H3PO4和NaF反应,发生强酸制取弱酸的反应;
(6)NH3比PH3更易液化,与氨气中含氢键、沸点高有关.
解答 解:I.(1)(1)Ca3(PO4)2含离子键、极性共价键,C含非极性共价键,发生化学变化时,离子键、极性共价键、非极性共价键均破坏,故答案为:abc;
(2)a.白磷与强碱发生自身氧化还原反应生成PH3、H2PO2-,故a不选;
b.白磷为非极性分子,易溶于CS2,故b不选;
c.白磷在空气中不能燃烧,则点燃时不能和氢气化合生成PH3,故c选;
d.着火点低,易自燃,故d不选;
故答案为:c;
(3)P4分子呈正四面体结构,含6个P-O键,每个面为等边三角形,键角为600,故答案为:6;600;
Ⅱ.(4)三聚磷酸可视为三个磷酸分子之间脱去两个水分子产物,其结构式为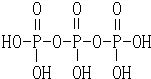 ,故答案为:;
,故答案为:;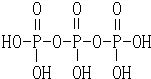 ;
;
(5)由K可知酸性的强弱,则少量H3PO4和NaF反应的离子方程式为H3PO4+F-=H2PO4-+HF,故答案为:H3PO4+F-=H2PO4-+HF;
(6)NH3比PH3更易液化,原因可能是氨气中含氢键、沸点高,与键能、分子间作用力无关,故答案为:c.
点评 本题考查弱电解质的电离、化学键等,为高频考点,把握化学键及化学反应的关系、物质结构、酸性比较为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度中等.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
15.生活中常用一些化学知识,下列分析或结论正确的是( )
| A. | 加碘食盐中添加的是碘化钾 | |
| B. | 将甲醛稀溶液喷在白菜上可以保鲜 | |
| C. | 牛奶中掺入三聚氰胺可以提高蛋白质含量 | |
| D. | 人体中维持血液的pH值稳定的主要离子是HCO3- |
16.下列说法正确的是( )
| A. | 乙烯和聚乙烯都能使溴水褪色 | |
| B. | 用新制的氢氧化铜浊液不能检验淀粉和纤维素是否发生了水解 | |
| C. | 油脂的水解反应,都是皂化反应 | |
| D. | 橄榄油、茶籽油和花生油等都能使溴水褪色 |
20.某蓝色手柄滴定管滴定后读数如图所示,则以下记录的数据正确的是( )


| A. | 20.00mL | B. | 20.0mL | C. | 20.10mL | D. | 20.1mL |
10.下列指定反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:2H++SO32-═SO2↑+H2O | |
| B. | 向Al2(SO4)3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O | |
| D. | 向0.1mol/LpH=1的KHA溶液中加入KOH溶液:H++OH-═H2O |
17.用密度为1.32g/cm3的硫酸溶液逐滴滴入到BaCl2溶液中,直到沉淀完全为止.已知所生成的溶液的质量等于原BaCl2溶液的质量,则H2SO4溶液的浓度为( )
| A. | 21.9% | B. | 43.1% | C. | 13.5mol/L | D. | 5.67mol/L |
14.某可逆反应过程的能量变化如图所示,下列说法正确的是( )
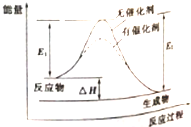

| A. | 该反应能量变化类型与CaCO3分解反应相同 | |
| B. | 加催化剂后,正反应速率加快,逆反应速率减小 | |
| C. | 若该反应为氧化还原反应,则可以将其设计成原电池 | |
| D. | 反应热△H=E2-E1 |
17.下列说法正确的是( )
| A. | 淀粉和纤维素均可以有(C6H10O5)n表示,因此它们互为同分异构体 | |
| B. | 17g羟基中所含电子的物质的量为9mol | |
| C. | 铁位于元素周期表中第四周期第ⅧB族 | |
| D. | 氨、塑料和橡胶都是以石油化工为基础的三大合成材料 |