题目内容
17.下列说法正确的是( )| A. | 淀粉和纤维素均可以有(C6H10O5)n表示,因此它们互为同分异构体 | |
| B. | 17g羟基中所含电子的物质的量为9mol | |
| C. | 铁位于元素周期表中第四周期第ⅧB族 | |
| D. | 氨、塑料和橡胶都是以石油化工为基础的三大合成材料 |
分析 A、淀粉和纤维素的n值不同;
B、求出-OH的物质的量,然后根据1mol-OH中含9mol电子来分析;
C、铁属于过渡元素;
D、合成纤维、合成塑料和合成橡胶是三大合成材料.
解答 解:A、淀粉和纤维素的n值不同,即分子式不同,故不是同分异构体,故A错误;
B、17g-OH的物质的量为1mol,而1mol-OH中含9mol电子,故B正确;
C、铁属于过渡元素,是第26号元素,处于第四周期第VIII族,故C错误;
D、合成纤维、合成塑料和合成橡胶是三大合成材料,氨不是三大合成材料之一,故D错误.
故选B.
点评 本题考查了三大合成材料、物质中电子数的计算和元素在周期表中的位置等问题,难度不大,应注意的是铁位于第VIII族,而非第VIIIB族.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5. 磷元素的单质及其化合物在生产和生活中有着广泛的应用.
磷元素的单质及其化合物在生产和生活中有着广泛的应用.
I.用磷矿石在高温下制备白磷(P4)的化学方程式为:2Ca3(PO4)2(s)+10C(s)→P4(g)+6CaO(s)+10CO(g)
(1)反应中破坏的化学键有abc.
a.离子键 b.极性共价键 c.非极性共价键
(2)白磷肯定不具有的性质是c(单项选择).
a.与强碱发生自身氧化还原反应 b.易溶于CS2
c.点燃时和氢气化合生成PH3 d.易自燃
(3)P4分子呈正四面体结构,分子中有6个P-P键,键角为600.
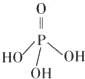
Ⅱ.磷酸分子结构式见图.三聚磷酸可视为三个磷酸分子之间脱去两个水分子产物,其结构式为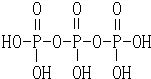 .
.
(5)根据上表数据,写出在溶液中少量H3PO4和NaF反应的离子方程式H3PO4+F-=H2PO4-+HF.
(6)NH3比PH3更易液化,原因可能是c(单项选择).
a.H-N键键能大于H-P键键能
b.NH3分子间范德华力大于PH3分子间范德华力
c.其它原因.
 磷元素的单质及其化合物在生产和生活中有着广泛的应用.
磷元素的单质及其化合物在生产和生活中有着广泛的应用.I.用磷矿石在高温下制备白磷(P4)的化学方程式为:2Ca3(PO4)2(s)+10C(s)→P4(g)+6CaO(s)+10CO(g)
(1)反应中破坏的化学键有abc.
a.离子键 b.极性共价键 c.非极性共价键
(2)白磷肯定不具有的性质是c(单项选择).
a.与强碱发生自身氧化还原反应 b.易溶于CS2
c.点燃时和氢气化合生成PH3 d.易自燃
(3)P4分子呈正四面体结构,分子中有6个P-P键,键角为600.
Ⅱ.磷酸分子结构式见图.三聚磷酸可视为三个磷酸分子之间脱去两个水分子产物,其结构式为
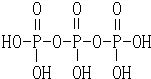 .
.| 电离常数(25℃) |
| HF:Ki=3.6×10 -4 |
| H3PO4:Ki1=7.5×10 -3, Ki2=6.2×10 -8,Ki3=2.2×10 -13 |
(6)NH3比PH3更易液化,原因可能是c(单项选择).
a.H-N键键能大于H-P键键能
b.NH3分子间范德华力大于PH3分子间范德华力
c.其它原因.
6.下列叙述正确的是( )
| A. | 油脂在酸的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| B. | 在水溶液里,乙酸分子中的-CH3可以电离出H+ | |
| C. | 一定条件下,氨基酸之间能发生反应,合成更复杂的化合物(多肽) | |
| D. | 向2ml苯中加入1ml酸性高锰酸钾溶液,振荡后静置,可观察到液体分层,上层呈紫红色 |
12.最简式相同,但既不是同系物又不是同分异构体的是( )
| A. | CH≡CH 和 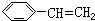 | B. | 甲醚和乙醇 | C. | 环丙烷和环己烷 | D. |  和 和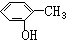 |
2.在下列氧化还原反应中,溴单质既做氧化剂又做还原剂的是( )
| A. | Br2+2NaI=2NaBr+I2 | |
| B. | 2P+8H2O+5Br2=2H3PO4+10HBr↑ | |
| C. | 3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑ | |
| D. | SO2+2H2O+Br2=H2SO4+2HBr |
9.下列关于硅单质及其化合物的说法,正确的是( )
①硅酸钠可用于制备木材防火剂
②硅是构成一些岩石和矿物的基本元素
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷,水晶,玻璃等是人类应用很早的硅酸盐材料.
①硅酸钠可用于制备木材防火剂
②硅是构成一些岩石和矿物的基本元素
③高纯度的硅单质广泛用于制作光导纤维
④陶瓷,水晶,玻璃等是人类应用很早的硅酸盐材料.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③④ |
6.元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为氩,氧化性最弱的简单阳离子是(填离子符号)Na+.
(3)已知:
①工业制镁时,电解MgCl2而不电解MgO的原因是MgO的熔点高,熔融时消耗更多能量,增加生产成本;
②制铝时,电解Al2O3而不电解AlCl3的原因是氯化铝是共价化合物,熔融态氯化铝难导电; ③写出电解Al2O3反应方程式2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$+4Al+3O2↑.
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为氩,氧化性最弱的简单阳离子是(填离子符号)Na+.
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
②制铝时,电解Al2O3而不电解AlCl3的原因是氯化铝是共价化合物,熔融态氯化铝难导电; ③写出电解Al2O3反应方程式2Al2O3(熔融)$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$+4Al+3O2↑.
7.下列物质没有固定沸点的是( )
| A. | 氯仿 | B. | 汽油 | C. | 硝基苯 | D. | 甲醇 |