题目内容
11.反应C(s)+H2O(g)?CO(g)+H2(g)在一体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )| A. | 保持体积不变,充入水蒸气使体系压强增大 | |
| B. | 将容器体积缩小一倍 | |
| C. | 增加C的量 | |
| D. | 加入催化剂 |
分析 A、体积不变,充入水使体系压强增大,加压速率加快;
B、体积缩小,反应体系中物质的浓度增大,化学反应速率越快;
C、根据浓度越大,化学反应速率越快,固体量的增减不影响反应速率;
D、加催化剂反应速率加快.
解答 解:A、保持体积不变,充入水蒸气,水蒸气参与反应,反应体系中的物质的浓度增加,则反应速率加快,故A错误;
B、将容器的体积缩小一半,反应体系中物质的浓度增大,则化学反应速率增大,故B错误;
C、因浓度越大,化学反应速率越快,但是固体量的增减不影响反应速率,所以增加C(s)的量,反应速率不变,故C正确;
D、加入催化剂,则反应速率增加,故D错误.
故选C.
点评 影响化学速率的因素有:温度、浓度、压强、催化剂、固体表面积,需要注意的是改变纯固体或液体的量,对反应速率无影响,压强改变必须引起浓度的改变才能引起化学反应速率的改变.

练习册系列答案
相关题目
1.某无色溶液中一定能大量共存的离子是( )
| A. | H+、Na+、NO3-、CO32- | B. | Na+、CO32-、Cu2+、Cl- | ||
| C. | K+、Na+、Cl-、NH4+ | D. | K+、Cl-、Ba2+、SO42- |
2.下列有关说法正确的是( )
| A. | 工业上现在大规模采用电解熔融NaCl或AlCl3制取Na或Al | |
| B. | 若电工操作中将铝线与铜线直接相连,会导致铜线更快被氧化 | |
| C. | 某反应的平衡常数K300℃>K350℃,则该反应△H<0 | |
| D. | 合成氨生产中将NH3液化分离,目的是加快正反应速率,提高H2的转化率 |
19.某试液中只可能含有K+、NH4+、Fe2+、Fe3+、Cl-、SO42-、NO3-、AlO2- 中的若干种离子,离子浓度均为0.1mol•L-1,某同学进行了如下实验:
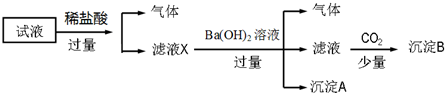
下列说法正确的是( ):

下列说法正确的是( ):
| A. | 原溶液中一定存在的离子为NH4+、Fe2+、NO3-和SO42- | |
| B. | 无法确定原试液中是否含有Fe3+、K+ | |
| C. | 滤液X中大量存在的阳离子有NH4+、Fe3+、H+和Al3+ | |
| D. | 无法确定沉淀B的成分 |
16.下列说法正确的是( )
| A. | 需要加热的化学反应都是吸热反应 | |
| B. | 水力发电是将化学能转化为电能的过程 | |
| C. | 可以通过化学反应完成16O到18O的转变 | |
| D. | 生铁、不锈钢、青铜都属于合金 |
3.下列有机物发生的反应属于还原反应的是( )
| A. | 乙醛与新制氢氧化铜反应 | B. | 油脂的氢化反应 | ||
| C. | 乙酸乙酯酸性条件下水解 | D. | 油脂的皂化反应 |
20.已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数c>d | B. | 非金属性Y<Z | ||
| C. | 氢化物的稳定性H2Y>HZ | D. | 原子半径W>X |
1.单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法不正确的是( )


| A. | 单斜硫和正交硫互为同素异形体 | |
| B. | 单斜硫比正交硫稳定 | |
| C. | 两种硫的燃烧反应均为放热反应 | |
| D. | S(s,单斜)=S(s,正交)△H=-0.33 kJ•mol-1 |