题目内容
16.下列说法正确的是( )| A. | 需要加热的化学反应都是吸热反应 | |
| B. | 水力发电是将化学能转化为电能的过程 | |
| C. | 可以通过化学反应完成16O到18O的转变 | |
| D. | 生铁、不锈钢、青铜都属于合金 |
分析 A.吸热反应实质是反应物所具有的总能量低于生成物所具有的总能量;
B.水力发电是将重力势能转化为电能的过程;
C.16O到18O的转变,为核变化;
D.合金是由两种或两种以上的金属与金属(或非金属)经一定方法熔合而成的具有金属特性的物质.结合各物质的成分判断.
解答 解:A.放热反应有的需加热,有的不需加热.如木炭的燃烧是一个放热反应,但需要点燃,点燃的目的是使其达到着火点.再如铝热反应也是,故A错误;
B.水力发电是将重力势能转化为电能的过程,故B错误;
C.16O到18O的转变,为核变化,不属于化学变化,故C错误;
D.生铁的主要成分是铁与碳,属于合金,不锈钢是在碳素钢中加入铬、锰、钨、镍、硅、钴等合金元素,属于合金,青铜主要含有铜、锡、铅等,属于合金,故D正确;
故选D.
点评 本题考查了吸热反应、能量的转化、核变化、合金等知识,注重基础知识的考查,选项B为易错点,题目难度不大.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
6.通常情况下,氯化钠、氯化艳、二氧化碳和二氧化硅的晶体结构分别如图所示:
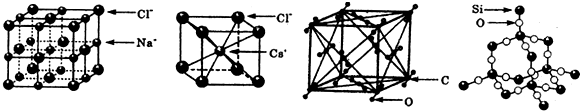
下列关于这些晶体结构和性质的叙述不正确的是( )

下列关于这些晶体结构和性质的叙述不正确的是( )
| A. | 干冰的晶胞中含有6个CO2分子 | |
| B. | 干冰是分子晶体,其中不仅存在分子间作用力,而且也存在共价键 | |
| C. | 在二氧化硅晶体中,平均每个Si原子形成4个Si-O共价单键 | |
| D. | 同一主族的元素与另一相同元素所形成的化学式相似的物质不一定具有相同的晶体结构 |
11.反应C(s)+H2O(g)?CO(g)+H2(g)在一体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| A. | 保持体积不变,充入水蒸气使体系压强增大 | |
| B. | 将容器体积缩小一倍 | |
| C. | 增加C的量 | |
| D. | 加入催化剂 |
1.有A、B、C、D、E五种短周期元素,其元素特征信息如下表:
回答下列问题:
(1)写出下列元素的最高价氧化物对应的水化物的化学式C、NaOH,D、Al(OH)3,E、HClO4;
(2)实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为共价键;
(3)E单质与C的氧化物对应水化物溶液反应的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
(4)A单质在E单质中燃烧的反应现象是安静的燃烧,苍白色火焰,产生白雾.
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
(1)写出下列元素的最高价氧化物对应的水化物的化学式C、NaOH,D、Al(OH)3,E、HClO4;
(2)实验测得DE3在熔融状态下不导电,则DE3中含有的化学键类型为共价键;
(3)E单质与C的氧化物对应水化物溶液反应的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
(4)A单质在E单质中燃烧的反应现象是安静的燃烧,苍白色火焰,产生白雾.
8.下列化学用语表述一定正确的是( )
| A. | 甲醛的电子式: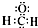 | |
| B. | 苯酚钠溶液中中通入少量二氧化碳气体: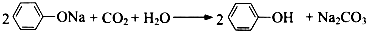 | |
| C. | 溴乙烷与氢氧化钠水溶液共热:C2H5Br+OH-$→_{△}^{H_{2}O}$CH2=CH2↑+Br-+H2O | |
| D. | 乙醇与灼热的氧化铜反应:CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O |
5.硒为第四周期VIA族元素,根据它在周期表中位置推测,硒不可能具有的性质( )
| A. | 单质有还原性 | B. | 硒元素在化合物中可显-2价 | ||
| C. | 硒化氢水溶液显弱碱性 | D. | 最高价氧化物的水化物显酸性 |
6.表是几种常用燃料的燃烧热:1mol燃料完全燃烧(生成物中的H2O为液态)时放出的热量.
(1)从热量角度分析,目前最适合家庭使用的优质气体燃料是甲烷.
(2)写出乙醇完全燃烧的热化学方程式C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1367KJ/mol.
| 物质 | 炭粉 | 一氧化碳 | 氢气 | 甲烷 | 乙醇 |
| 状态 | 固体 | 气体 | 气体 | 气体 | 液体 |
| 热量(kJ) | 392.8 | 282.6 | 285.8 | 890.3 | 1367 |
(2)写出乙醇完全燃烧的热化学方程式C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=-1367KJ/mol.
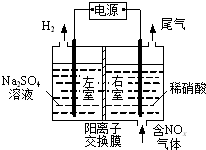 电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).
电解法处理含氮氧化物废气,可回收硝酸,具有较高的环境效益和经济效益.实验室模拟电解法吸收NOx的装置如图所示(图中电极均为石墨电极).