题目内容
17.10gNaOH溶解于90g水中,溶液内含有H元素的物质的量是( )| A. | 0.25mol | B. | 10.25mol | C. | 10mol | D. | 0.5mol |
分析 根据n=$\frac{m}{M}$计算NaOH、水的物质的量,溶液中H元素包含NaOH与水中H元素,结合化学式计算H元素的物质的量.
解答 解:溶液中H元素包含NaOH与水中的H元素,则溶液中H元素质量为$\frac{10}{40g/mol}$+$\frac{90g}{18g/mol}$×2=10.25mol,
故选:B.
点评 本题考查物质的量有关计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
7.用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质(括号内),溶液一定不能与原来溶液一样的是( )
| A. | CuCl2(CuCl2) | B. | AgNO3(Ag2O) | C. | NaCl(NaCl) | D. | CuSO4[Cu(OH)2] |
8.下列实验操作正确的是( )
| A. |  酸式滴定管排气泡 | B. |  配制100 mL 0.01mol/L盐酸 | ||
| C. | 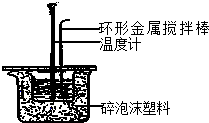 测定中和热 | D. |  验证铁与水蒸气反应生成气体 |
12.NaNO2是一种食品添加剂,能致癌.酸性KMnO4溶液与NaNO2反应的离子方程式是:MnO4-+NO2-+□→Mn2++NO3-+H2O (未配平),下列叙述中正确的是( )
| A. | 该反应中NO2-被还原 | |
| B. | 生成1mol NaNO3需消耗0.4mol KMnO4 | |
| C. | 反应过程中溶液的pH减小 | |
| D. | □中的粒子是OH- |
9.对于在密闭容器中进行的可逆反应2SO2(g)+18O2(g)?2SO3(g),下列说法正确的是( )
| A. | 容器内只含有18O2、SO2、SO3三种分子 | |
| B. | 18O只存在18O2分子中 | |
| C. | 容器内含有18O2、S18O2、S18O3等分子 | |
| D. | 反应达到限度时,容器内只含有18O2、S18O2、S18O3分子 |
7.下列叙述不正确的是( )D工业上电解饱和食盐水的.
| A. | 铁表面镀锌,锌作阳极 | |
| B. | 船底镶嵌锌块,锌作正极,以防船体被腐蚀 | |
| C. | 钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-═4OH- | |
| D. | 工业上电解饱和食盐水的阳极反应:2Cl--2e-═Cl2↑ |