题目内容
9.对于在密闭容器中进行的可逆反应2SO2(g)+18O2(g)?2SO3(g),下列说法正确的是( )| A. | 容器内只含有18O2、SO2、SO3三种分子 | |
| B. | 18O只存在18O2分子中 | |
| C. | 容器内含有18O2、S18O2、S18O3等分子 | |
| D. | 反应达到限度时,容器内只含有18O2、S18O2、S18O3分子 |
分析 该反应为可逆反应,SO2和O2反应生成SO3的同时,SO3分解生成SO2和O2,可逆反应不会进行彻底.
解答 解:该反应为可逆反应,在混合气体中充入一定量的18O2,SO2和18O2反应生成SO3中含有18O,同时SO3分解生成SO2和O2,则SO2中含有18O原子,则18O原子存在于O2、SO2和SO3中,根据可逆反应不会进行彻底,2mol SO2和1mol18O2在一定条件下,不会全部转化为三氧化硫,即生成三氧化硫的量小于2mol,
A.18O原子存在于O2、SO2和SO3中,故A错误;
B.SO2和18O2反应生成SO3中含有18O,同时SO3分解生成SO2和O2,18O原子存在于O2、SO2和SO3中,故B错误;
C.在混合气体中充入一定量的18O2,SO2和18O2反应生成SO3中含有18O,同时SO3分解生成SO2和O2,则SO2中含有18O原子,则18O原子存在于O2、SO2和SO3中,容器内含有18O2、S18O2、S18O3等分子,故C正确;
D.反应达到限度时,达到平衡状态,容器内含有18O2、S18O2、S18O3分子,还可能含有SO2、SO3分子,故D错误;
故选C.
点评 本题考查化学反应的可逆性,题目难度不大,注意可逆反应的特点,同位素原子在反应中的存在形式,此类题目易出错.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
19.X、Y、Z、T、V为5种短周期元素,X、Y、Z在周期表中位置如图所示.这3种元素 原子序数之和是41,X和T在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄 色固体)两种化合物.V单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使紫色石蕊溶液变 红,则:
(1)5种元素的元素符号分别是XO,YS,ZCl,TNa,VH.
(2)Y的原子结构示意图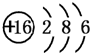 .
.
(3)T与X形成化合物T2X与T2X2的化学方程式分别为4Na+O2=2Na2O,2Na+O2=Na2O2.
| X | |
| Y | Z |
(2)Y的原子结构示意图
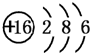 .
.(3)T与X形成化合物T2X与T2X2的化学方程式分别为4Na+O2=2Na2O,2Na+O2=Na2O2.
17.10gNaOH溶解于90g水中,溶液内含有H元素的物质的量是( )
| A. | 0.25mol | B. | 10.25mol | C. | 10mol | D. | 0.5mol |
4.铁单质及其化合物在生活、生产中应用广泛.请回答:
(1)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是Cu+2Fe3+=2Fe2++Cu2+.
(2)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2,若有1,.5mol Fe3O4参加反应,转移电子的物质的量是12mol.
(3)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是B(填字母).
(1)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是Cu+2Fe3+=2Fe2++Cu2+.
(2)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2,若有1,.5mol Fe3O4参加反应,转移电子的物质的量是12mol.
(3)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是B(填字母).
| 陈述Ⅰ | 陈述Ⅱ | 判断 | |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁表面形成致密氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对,有 |
14.体积不变的密闭容器中进行如下反应:X2(g)+3Y2(g)?2Z(g),X2、Y2、Z起始浓度分别为0.4mol•L-1、0.6mol•L-1、0.4mol•L-1,当平衡时,下列数据肯定不对的是( )
| A. | X2为0.5mol•L-1,Y2为1.0mol•L-1 | B. | Y2为1.0mol•L-1 | ||
| C. | X2为0.5mol•L-1,Z为0.2mol•L-1 | D. | Z为0.6mol•L-1 |
18.某溶液里存有NH4+Fe3+ Cu2+ Cl- SO42-离子,溶液不浑浊的是( )
| A. | CuCl2 NH4Cl Fe2(SO4)3 NaNO3 | |
| B. | (NH4)2SO4 CuSO4 Na2CO3 FeCl3 | |
| C. | Cu(NO3)2 NH4 NO3 FeCl3 H2S | |
| D. | Ba Cl2 Cu(NO3)2 (NH4)2SO4 Fe (NO3)3 |
19.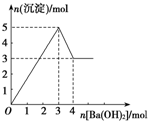 如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
 如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )| A. | MgSO4 | B. | KAl(SO4)2 | C. | Al2(SO4)3 | D. | Na AlO2 |