题目内容
7.用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质(括号内),溶液一定不能与原来溶液一样的是( )| A. | CuCl2(CuCl2) | B. | AgNO3(Ag2O) | C. | NaCl(NaCl) | D. | CuSO4[Cu(OH)2] |
分析 用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质(括号内),溶液一定不能与原来溶液一样,说明加入物质不是析出物质,据此分析解答.
解答 解:A.电解氯化铜溶液时,阳极上氯离子放电、阴极上铜离子放电,所以析出的物质相当于氯化铜,则加入氯化铜即可恢复原状,故A不选;
B.电解硝酸银溶液时,阳极上氢氧根离子放电生成氧气、阴极上银离子放电生成Ag,相当于析出氧化银,所以加入氧化银即可使溶液恢复原状,故B不选;
C.电解氯化钠溶液时,阳极上析出氯气、阴极上析出氢气,要使溶液恢复原状,应该通入适量氯化氢即可,所以加入NaCl不能使溶液恢复原状,故C选;
D.电解硫酸铜溶液时,阳极上氢氧根离子放电生成氧气,阴极上铜离子放电生成Cu,当铜离子完全放电时,阴极上氢离子放电生成氢气,所以相当于析出氢氧化铜,应该加入氢氧化铜即可恢复原状,故D不选;
故选C.
点评 本题考查电解原理,为高频考点,明确离子放电顺序是解本题关键,根据“析出什么、加入什么”原则分析解答,易错选项是D,注意该选项是既电解硫酸铜还电解水,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| B. | 1.5molNO2与足量H2O反应,转移的电子数为1.5NA | |
| C. | 常温常压下,46gNO2和N2O4混合气体含有的原子数为3NA | |
| D. | 含有H2SO41mol的浓硫酸与足量铜反应,生成SO2的分子数为0.5NA |
2.甲、乙、丙、丁分别是硫酸铝、硫酸铁、氢氧化钠、氯化钡等四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失.丁溶液滴入甲溶液中,无明显现象发生.据此可推断丙物质是( )
| A. | Fe2(SO4)3 | B. | NaOH | C. | Al2(SO4)3 | D. | BaCl2 |
19.X、Y、Z、T、V为5种短周期元素,X、Y、Z在周期表中位置如图所示.这3种元素 原子序数之和是41,X和T在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄 色固体)两种化合物.V单质在Z单质中燃烧产生苍白色火焰,产物溶于水能使紫色石蕊溶液变 红,则:
(1)5种元素的元素符号分别是XO,YS,ZCl,TNa,VH.
(2)Y的原子结构示意图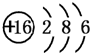 .
.
(3)T与X形成化合物T2X与T2X2的化学方程式分别为4Na+O2=2Na2O,2Na+O2=Na2O2.
| X | |
| Y | Z |
(2)Y的原子结构示意图
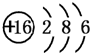 .
.(3)T与X形成化合物T2X与T2X2的化学方程式分别为4Na+O2=2Na2O,2Na+O2=Na2O2.
16.在一定温度下,向不同电解质溶液中加入新物质时,其电流强度(I)随新物质加入量(m)的变化曲线不正确
的是( )
的是( )
| A | B | C | D |
 |  |  | [ 来源:] 来源:] |
| 向Ba(OH)2溶液中逐滴加入等浓度的H2SO4至过量 | 向醋酸溶液中逐滴加入等浓度的氨水至过量 | 向盐酸溶液中逐滴加入等浓度的NaOH溶液至过量 | 向氨水中逐滴加入等浓度的盐酸至过量 |
| A. | A | B. | B | C. | C | D. | D |
17.10gNaOH溶解于90g水中,溶液内含有H元素的物质的量是( )
| A. | 0.25mol | B. | 10.25mol | C. | 10mol | D. | 0.5mol |