题目内容
10.除去溶解在苯中的少量苯酚,正确的方法是( )| A. | 过滤 | B. | 用分液漏斗分液 | ||
| C. | 通入足量CO2后,过滤 | D. | 加入适量NaOH溶液,反应后再分液 |
分析 苯酚与碱反应后,与苯分层,可分液分离,以此来解答.
解答 解:A.苯与苯酚互溶,不能过滤分离,故A错误;
B.苯与苯酚互溶,不能用分液漏斗分离,故B错误;
C.均与二氧化碳不反应,不能分离,故C错误;
D.苯酚与NaOH反应后,与苯分层,再分液可分离,故D正确;
故选D.
点评 本题考查混合物分离提纯,为高频考点,把握有机物的性质、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
7.已知一定温度压强下,N2(g)+3H2(g)?2NH3(g),△H=-92kJ/mol,在同温下向某定容密闭容器甲中通入1.0molN2和3.0molH2,反应完成时放出热量Q1kJ,向另一体积相同的定容密闭容器乙中通入1.5molN2和3.0molH2,相同条件下反应完成时放出热量为Q2kJ,则下列关系正确的是( )
| A. | 2Q2=Q1=92.4 | B. | Q2<Q1<92.4 | C. | Q1=Q2=92.4 | D. | Q1<Q2<92.4 |
5.下列物质能将品红氧化使品红溶液褪色的是( )
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫 ⑤漂白粉.
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫 ⑤漂白粉.
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ②③④ | D. | ②③⑤ |
15.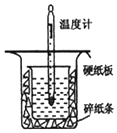 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从实验装置看,其中尚缺少的一种玻璃用品是环形玻璃搅拌器,
(2)若改用60mL 0.25mol•L-1H2SO4和50mL 0.55mol•L-1NaOH溶液进行反应与上述实验相比,所求中和热相等(填“相等”“不相等”)
(3)结合实验数据填空:
①由表中数据可知反应前后溶液的平均温度差,即t2-t1的均值为:3.5℃.
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-58.52 kJ/mol.
 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:| 序号 | 起始温度t1/℃ | 终止温度t2/℃ | t2-t1均值 | ||
| H2SO4 | NaOH | 均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29,6 | |
| 2 | 29.0 | 29.4 | 29,2 | 32.9 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
(2)若改用60mL 0.25mol•L-1H2SO4和50mL 0.55mol•L-1NaOH溶液进行反应与上述实验相比,所求中和热相等(填“相等”“不相等”)
(3)结合实验数据填空:
①由表中数据可知反应前后溶液的平均温度差,即t2-t1的均值为:3.5℃.
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-58.52 kJ/mol.
2.已知乙烷的燃烧热为1190KJ/mol,则下列表述正确的是( )
| A. | 2C2H6(g)+7O2 (g)=4CO2 (g)+6H2O(l);△H=-1190KJ/mol | |
| B. | C2H6(g)+$\frac{7}{2}$O2 (g)=2CO2 (g)+3H2O(g);△H=-1190KJ/mol | |
| C. | 298k、101kPa时,30g乙烷气体完全燃烧生成CO2气体和液态水,放出1190kJ热量 | |
| D. | 该反应中,反应物所具有的总能量小于生成物所具有的总能量 |
19.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 酒精和水 | B. | 水和四氯化碳 | C. | 汽油和植物油 | D. | 四氯化碳和苯 |