题目内容
11.在葡萄糖溶液中有一种环状结构的分子和葡萄糖分子互为同分异构体,分子式也是C6H12O6.在溶液中它存在下列平衡: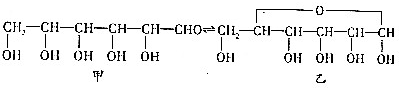
(1)上述平衡中的环状结构(乙)的分子是通过链状结构(甲)分子中的醛基和羟基之间发生加成反应而生成的.
(2)现要制备一种链状烃基醚
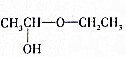 试写出由两种简单的有机物合成该烃基醚的化学方程式:CH3CHO+CH3CH2OH→
试写出由两种简单的有机物合成该烃基醚的化学方程式:CH3CHO+CH3CH2OH→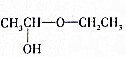 .
.(3)已知溴水(Br2+H2O)可将多径基醛中的醛基氧化.写出溴水与葡萄糖反应的化学方程式:C5H11O5CHO+H2O+Br2→C5H11O5COOH(葡萄糖酸)+2HBr.
分析 (1)比较葡萄糖的链状结构和环状结构可知,-CHO与第五个碳原子上的-OH加成而将链状结构变成了环状结构,也可以说是醛基与醇羟基加成生成了醚键;
(2)根据该反应原理可推知,用CH3CHO和CH3CH2OH即可制得此链羟基醚;
(3)葡萄糖中的醛基被溴水氧化成羧基,生成葡萄糖酸和溴化氢.
解答 解:(1)比较葡萄糖的链状结构和环状结构可知,-CHO与第五个碳原子上的-OH加成而将链状结构变成了环状结构.也可以说,是醛基与醇羟基加成生成了醚键,
故答案为:醛;羟;加成;
(2)根据该反应原理可推知,用CH3CHO和CH3CH2OH即可制得此链羟基醚,方程式为:CH3CHO+CH3CH2OH→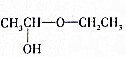 ,
,
故答案为:CH3CHO+CH3CH2OH→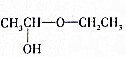 ;
;
(3)葡萄糖中的醛基被溴水氧化成羧基,生成葡萄糖酸和溴化氢,反应方程式为:C5H11O5CHO+H2O+Br2→C5H11O5COOH(葡萄糖酸)+2HBr,
故答案为:C5H11O5CHO+H2O+Br2→C5H11O5COOH(葡萄糖酸)+2HBr.
点评 本题考查官能团决定有机物的主要化学性质,抓住官能团的变化,对比反应物和产物分析出反应原理,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.表是元素周期表的一部分,回答下列有关问题:
(1)画出原子的结构示意图:④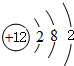 ,⑧
,⑧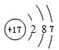
(2)第三周期(除稀有气体元素)中原子半径最大的元素是③(填序号),跟它同周期原子半径最小的元素是⑧(填序号)
(3)元素⑦与元素⑧相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)写出实验室制取元素①的气态氢化物最常用的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
(5)元素①的最高价氧化物对应的水化物的浓溶液与单质铜反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
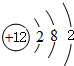 ,⑧
,⑧
(2)第三周期(除稀有气体元素)中原子半径最大的元素是③(填序号),跟它同周期原子半径最小的元素是⑧(填序号)
(3)元素⑦与元素⑧相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)写出实验室制取元素①的气态氢化物最常用的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
(5)元素①的最高价氧化物对应的水化物的浓溶液与单质铜反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
2.短周期主族元素X,Y,Z,W的原子序数依次增大,X原子核外最外层电子数是其电子层数的2倍,X,Y的核电荷数之比为3:4,W-的最外层为8电子结构,金属单质Z在空气中燃烧生成的化合物可与水发生氧化还原反应,下列说法正确的是( )
| A. | X与Y能形成多种化合物,一般条件下都能与Z的最高价氧化物的水化物发生反应 | |
| B. | 原子半径大小:X<Y,Z>W | |
| C. | 化合物Z2Y和ZWY3都只存在离子键 | |
| D. | Y,W的某些单质或两元素之间形成的某些化合物可作水的消毒剂 |
19.下列图象能正确表示化学实验的进程或结果的是( )
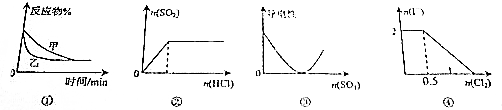

| A. | 图①表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 | |
| B. | 图②表示一定浓度的Na2SO3溶液中滴加稀盐酸,生成SO2与HCl的物质的量的关系 | |
| C. | 图③表示在Ba(OH)2溶液中加入SO3至过量的过程中溶液导电性的变化 | |
| D. | 图④表示在1L 1mol•L-1FeI2溶液中,通入Cl2时I-物质的量的变化 |
6.在1.01×105Pa、200℃下,将乙烯、乙醇、乙酸乙酯的混合气vL(已换算成标准状况,下同)在足量的氧气中充分燃烧后,恢复至1.01×105Pa、200℃,测得生成nL混合气(CO2与H2O),消耗氧气mL,下列关系正确的是( )
| A. | v>n | B. | m>n | C. | v<m | D. | 不能确定 |
16.下列叙述中,不正确的是( )
| A. | 2H与3H互为同位素 | B. | 金刚石与石墨互为同素异形体 | ||
| C. | 3O2$\frac{\underline{\;放电\;}}{\;}$2O3是物理变化 | D. | 乙醇与二甲醚互为同分异构体 |
6.下列说法正确的是( )
| A. | 有机物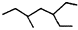 的系统命名为:3-乙基-5-甲基庚烷 的系统命名为:3-乙基-5-甲基庚烷 | |
| B. | 用Na2CO3溶液能区分CH3COOH、CH3CH2OH、苯、硝基苯四种物质 | |
| C. | 等质量的丁烷、丁烯、1,3-丁二烯分别充分燃烧,所耗氧气的量依次增加 | |
| D. | 糖类、油脂、蛋白质都属于天然有机高分子化合物,都能发生水解反应 |
3.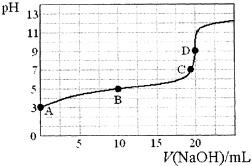 已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
 已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )
已知:H3PO2是一元中强酸.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图,则下列说法不正确的是( )| A. | H3PO2的电离方程式为:H3PO2?H2PO2-+H+ | |
| B. | 常温下,Ka(H3PO2)≈10-5 | |
| C. | 该滴定实验中,用酚酞作指示剂比用甲基橙作指示剂的误差小 | |
| D. | B点溶液中存在关系:c(H+)+c(H3PO2)=c(OH-)+c(H2PO2-) |
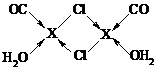 .
.