题目内容
19.下列图象能正确表示化学实验的进程或结果的是( )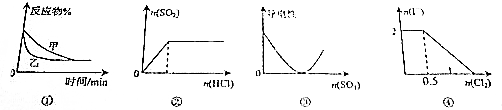
| A. | 图①表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 | |
| B. | 图②表示一定浓度的Na2SO3溶液中滴加稀盐酸,生成SO2与HCl的物质的量的关系 | |
| C. | 图③表示在Ba(OH)2溶液中加入SO3至过量的过程中溶液导电性的变化 | |
| D. | 图④表示在1L 1mol•L-1FeI2溶液中,通入Cl2时I-物质的量的变化 |
分析 A.图①应是催化剂对反应速率的影响;
B.一定浓度的Na2SO3溶液中滴加稀盐酸,开始无气体生成,亚硫酸钠和盐酸反应生成亚硫酸氢钠和氯化钠,全部变化为碳酸氢钠后,继续滴加盐酸放出二氧化硫;
C.根据Ba(OH)2溶液和稀硫酸反应生成硫酸钡沉淀以及纯水几乎不导电进行解答;
D.I-还原性大于Fe2+,通入Cl2时先氧化碘离子生成碘单质,碘离子全部被氧化后,继续通入氯气氧化亚铁离子;
解答 解:A.图①中甲乙反应速率不同,但平衡状态相同,由于反应中反应前后气体计量数不同,改变压强平衡发生移动,应为催化剂的影响,故A错误;
B.一定浓度的Na2SO3溶液中滴加稀盐酸,开始无气体生成,亚硫酸钠和盐酸反应生成亚硫酸氢钠和氯化钠,Na2SO3+HCl=NaHSO3+NaCl,全部变化为碳酸氢钠后,继续滴加盐酸放出二氧化硫,NaHSO3+HCl=NaCl+H2O+SO2↑,图象变化不符合,故B错误;
C.加入SO3和水反应生成硫酸,Ba(OH)2溶液和稀硫酸反应生成硫酸钡沉淀,纯水几乎不导电,所以烧杯中溶液导电性逐渐减弱,当恰好反应时导电性0,再继续滴加稀硫酸,溶液中的自由移动的离子增加,导电性逐渐增强,与图象相符,故C正确;
D.I-还原性大于Fe2+,通入Cl2时先氧化碘离子生成碘单质,碘离子全部被氧化后,继续通入氯气氧化亚铁离子,图象不符合,故D错误;
故选C.
点评 本题考查了实验过程和图象变化的分析判断,主要是催化剂作用、盐类水解、酸碱反应后溶液的导电性、氧化还原反应等,掌握基础是解题关键,题目难度中等.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
10.X、Y、Z、W是原子序数逐渐增大的四种短周期主族元素,其原子半径如下表,已知Y、Z两种元素的单质是空气主要成分,W原子最外层电子数与Ne原子最外层电子数相差1.下列说法正确的是( )
| 元素 | X | Y | Z | W |
| 原子半径/nm | 0.037 | 0.075 | 0.074 | 0.099 |
| A. | Y、Z、W处于周期表中同一周期 | B. | 通常状况下得不到纯净的YZ2 | ||
| C. | X与Z形成的化合物不含非极性键 | D. | X、Z、W形成的化合物为弱酸 |
7.(1)三种弱酸HA、H2B、HC,电离平衡常数的数值为:①1.8×10-5、②5.6×10-11、③4.9×10-10、④4.3×10-7(数据顺序已打乱),已知三种酸和它们的盐之间能发生以下反应:
①HA+HB-(少量)=A-+H2B,②H2B(少量)+C-=HB-+HC,③HA(少量)+C-=A-+HC..则三种酸对应的电离平衡常数分别为(请填空)
(2)常温下0.1mol/LCH3COOH溶液加水稀释过程,下列表达式数据一定变小的是A.
A.c(H+) B.c(H+)•c(OH-) C.$\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$ D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(3)体积为10mLpH=2醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化分别为HX3.6、CH3COOH3.2,则HX电离平衡常数大于(填大于、等于或小于)醋酸平衡常数;理由是因为稀释相同倍数,HX的pH变化比CH3COOH大,即HX更易电离,所以HX电离平衡常数也大.
①HA+HB-(少量)=A-+H2B,②H2B(少量)+C-=HB-+HC,③HA(少量)+C-=A-+HC..则三种酸对应的电离平衡常数分别为(请填空)
| HA | H2B | HC | ||
| Ka | K${\;}_{{a}_{1}}$ | K${\;}_{{a}_{2}}$ | K${\;}_{{a}_{3}}$ | K${\;}_{{a}_{4}}$ |
| 数值 | ||||
A.c(H+) B.c(H+)•c(OH-) C.$\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$ D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(3)体积为10mLpH=2醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化分别为HX3.6、CH3COOH3.2,则HX电离平衡常数大于(填大于、等于或小于)醋酸平衡常数;理由是因为稀释相同倍数,HX的pH变化比CH3COOH大,即HX更易电离,所以HX电离平衡常数也大.
14.滴定分析中,称样量在0.1g以上,相对含量大于1%的分析称为( )
| A. | 微量分析 | B. | 半微量分析 | C. | 痕量分析 | D. | 常量分析 |
12.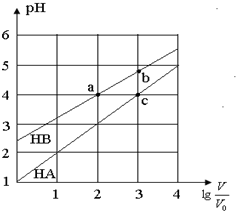 常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述正确的是( )
常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述正确的是( )
 常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述正确的是( )
常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述正确的是( )| A. | 该温度下HB的电离平衡常数a<b | |
| B. | 溶液中水的电离程度:a=c>b | |
| C. | 相同条件下NaA溶液的pH小于NaB溶液的pH | |
| D. | 当lg$\frac{V}{{V}_{0}}$=3时,若同时微热两种溶液(不考虑HA、HB和H2O的挥发),则$\frac{c({B}^{-})}{c({A}^{-})}$减小 |
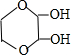 、
、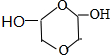 (任写一种)(不考虑立体异构)
(任写一种)(不考虑立体异构)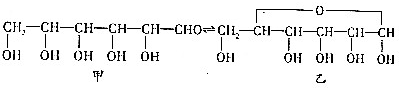
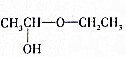 试写出由两种简单的有机物合成该烃基醚的化学方程式:CH3CHO+CH3CH2OH→
试写出由两种简单的有机物合成该烃基醚的化学方程式:CH3CHO+CH3CH2OH→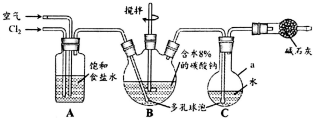 次氯酸(HClO)仅存在于溶液中,有很强的氧化性和漂白作用.某兴趣小组拟用Cl2O与潮湿Na2CO3反应制得Cl2O,再用水吸收Cl2O制备次氯酸溶液,并测定其浓度.
次氯酸(HClO)仅存在于溶液中,有很强的氧化性和漂白作用.某兴趣小组拟用Cl2O与潮湿Na2CO3反应制得Cl2O,再用水吸收Cl2O制备次氯酸溶液,并测定其浓度.