��Ŀ����
1������Ԫ�����ڱ���һ���֣��ش������й����⣺| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | �� | |
| 4 | �� | ⑪ | ⑫ |
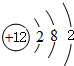 ����
����
��2���������ڣ���ϡ������Ԫ�أ���ԭ�Ӱ뾶����Ԫ���Ǣۣ�����ţ�������ͬ����ԭ�Ӱ뾶��С��Ԫ���Ǣࣨ����ţ�
��3��Ԫ�آ���Ԫ�آ���ȣ��ǽ����Խ�ǿ����Cl����Ԫ�ط��ű�ʾ�������б�������֤����һ��ʵ����b
a�������¢ߵĵ��ʺ͢�ĵ���״̬��ͬ
b������⻯��Ȣߵ��⻯���ȶ�
c��һ�������¢ߺ͢�ĵ��ʶ���������������Һ��Ӧ
��4��д��ʵ������ȡԪ�آٵ���̬�⻯����õĻ�ѧ����ʽCa��OH��2+2NH4Cl$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O
��5��Ԫ�آٵ�����������Ӧ��ˮ�����Ũ��Һ�뵥��ͭ��Ӧ�Ļ�ѧ����ʽΪCu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
���� ��Ԫ�������ڱ���λ�ã���֪��ΪN����ΪF����ΪNa����ΪMg����ΪAl����ΪSi����ΪS����ΪCl����ΪAr����ΪK��⑪ΪCa��⑫ΪBr��
��1����ΪMg��������Ϊ12��ԭ�Ӻ�����12�����ӣ���3�����Ӳ㣬���������Ϊ2��8��2��
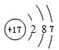
��ΪCl��������Ϊ17��ԭ�Ӻ�����17�����ӣ���3�����Ӳ㣬���������Ϊ2��8��7��
��2��ͬ���������������Ԫ�ص�ԭ�Ӱ뾶��С��
��3��ͬ����������ҷǽ�������ǿ�����Ը��ݵ�����������Ӧ���׳̶ȡ��⻯���ȶ��ԣ���ۺ���������ԡ�����֮�����û����жϣ�
��4��Ԫ�آٵ���̬�⻯��ΪNH3��ʵ�������Ȼ�������������ڼ����������Ʊ���������Ӧ�������Ȼ�����ˮ��
��5��Ԫ�آٵ�����������Ӧ��ˮ����Ϊ���ᣬCu��Ũ���ᷴӦ��������ͭ������������ˮ��
��� �⣺��Ԫ�������ڱ���λ�ã���֪��ΪN����ΪF����ΪNa����ΪMg����ΪAl����ΪSi����ΪS����ΪCl����ΪAr����ΪK��⑪ΪCa��⑫ΪBr��
��1����ΪMg��ԭ�Ӻ�����12�����ӣ���3�����Ӳ㣬���������Ϊ2��8��2��ԭ�ӽṹʾ��ͼΪ��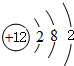 ��
��
��ΪCl��ԭ�Ӻ�����17�����ӣ���3�����Ӳ㣬���������Ϊ2��8��7��ԭ�ӽṹʾ��ͼΪ�� ��
��
�ʴ�Ϊ��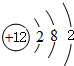 ��
�� ��
��
��2��ͬ���������������Ԫ�ص�ԭ�Ӱ뾶��С���ʵ������ڣ���ϡ������Ԫ�أ���ԭ�Ӱ뾶����Ԫ���� �ۣ�����ͬ����ԭ�Ӱ뾶��С��Ԫ���Ǣ࣬
�ʴ�Ϊ���ۣ��ࣻ
��3��S��Clͬ���ڣ�������ҷǽ�������ǿ����ClԪ�طǽ����Խ�ǿ���ɸ����⻯����ȶ����жϣ����ʵ�״̬�����������ʣ����ܱȽϷǽ�����ǿ�������ʶ������������Ʒ�Ӧ��Ҳ�������ڱȽϷǽ����ԣ�
�ʴ�Ϊ��Cl��b��
��4��Ԫ�آٵ���̬�⻯��ΪNH3��ʵ�������Ȼ�������������ڼ����������Ʊ���������Ӧ�������Ȼ�����ˮ����Ӧ����ʽΪ��Ca��OH��2+2NH4Cl$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��Ca��OH��2+2NH4Cl$\frac{\underline{\;\;��\;\;}}{\;}$CaCl2+2NH3��+2H2O��
��5��Ԫ�آٵ�����������Ӧ��ˮ����Ϊ���ᣬCu��Ũ���ᷴӦ��������ͭ������������ˮ����Ӧ����ʽΪ��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
�ʴ�Ϊ��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɣ����ضԻ�ѧ���Ԫ���������Լ�Ԫ�ػ�����֪ʶ�Ŀ��飬ע���������Ԫ�����ڱ��ṹ�����ս����ԡ��ǽ�����ǿ���Ƚ�ʵ����ʵ��

| A�� | �ء��ơ�þ�Ȼ��ý����Ż�ʱ����������ĭ�������� | |
| B�� | ̽���¶ȶ���������������ᷴӦ���ʵ�Ӱ��ʱ�����Ƚ�������Һ��ϲ���ʱ������ˮԡ�������趨�¶ȣ����õķ�Ӧ����ƫ�� | |
| C�� | ������Ϻ�Ӧ��ֹͣ���ȣ���װ����ȴ��ֹͣͨˮ���ٲ�ж����װ�� | |
| D�� | Ϊȷ����һ�����ʵ���Ũ�ȵ���Һ�����ݹ�����������ƿ�ڼ�����ˮ���ӽ��̶���ʱ�����õιܼ�����ˮ���̶��� |
| A�� | ij���鳮���к��е����Һ�����ٳ�������ɫ��������������������������� | |
| B�� | �����°���������õ�����������Ҷľ��ԭ�ϵ���Ҫ�ɷ�����ά�� | |
| C�� | �Ž�����¬�����Լ���Ϊ�У�����Ϊ���ɣ����������ۡ�������ָ�������ĺϽ� | |
| D�� | ������һ�գ���ˮ�����գ���ȡ֭�����ù����Ƕ������ص���ȡ�����������仯 |

�����õ����й��������£�
| ��Է������� | �ܶȣ�g/cm3�� | �е�/�� | �ܽ��� | |
| ������ | 100 | 0.9618 | 161 | ����ˮ |
| ����ϩ | 82 | 0.8102 | 83 | ������ˮ |
��a�м���20g��������2СƬ���Ƭ����ȴ��������������1mLŨ���ᣮb��ͨ����ȴˮ��ʼ��������a�������������¶Ȳ�����90�森
�����ᴿ��
��Ӧ�ֲ��ﵹ���Һ©���зֱ�������5%̼������Һ��ˮϴ�ӣ�����������ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ƣ�����ͨ������õ���������ϩ10g��
�ش��������⣺
��1��װ��a��������������ƿ��
��2���������Ƭ�������Ƿ�ֹ���У��������һ��ʱ��������ǼӴ�Ƭ��Ӧ�ò�ȡ����ȷ������B������ȷ�𰸱�ţ���
A���������� B����ȴ�� C�����貹�� D����������
��3����Һ©����ʹ��ǰ����ϴ�ɾ�����©���ڱ�ʵ���������У�����Ӧ�ôӷ�Һ©�����Ͽڵ�������Ͽڵ��������¿ڷų�������
��4�������ᴿ�����м�����ˮ�Ȼ��Ƶ�Ŀ��������ˮ��
��5���ڻ���ϩ�ֲ�����������У������õ���������ABE������ȷ�𰸱�ţ���
AԲ����ƿ B�¶ȼ� C©�� D������ E������
��6����ʵ�����õ��Ļ���ϩ������61%����������λ��Ч���֣�
��ע������=$\frac{ʵ�ʲ���}{���۲���}$��100%��
| A�� | �٢� | B�� | �ۢ� | C�� | �٢ۢ� | D�� | ȫ�� |
��ϢA����һ������I1��ָ��̬ԭ��X��g�����ڻ�̬ʱ��ʧȥһ�����ӳ�Ϊ��̬������X+��g���������������ͼ�Dz���Ԫ��ԭ�ӵĵ�һ������I1��ԭ�������仯������ͼ������12�š�17��Ԫ�ص��й�����ȱʧ����

��ϢB����ͬԪ�ص�ԭ���ڷ������������ӵ�������С���õ縺�Ա�ʾ��һ����Ϊ����������ɼ�ԭ�Ӽ�ĵ縺�Բ�ֵ����1.7��ԭ��֮��ͨ���γ����Ӽ�����������ɼ�ԭ�Ӽ�ĵ縺�Բ�ֵС��1.7��ͨ���γɹ��ۼ�������ijЩԪ�صĵ縺��ֵ��
| Ԫ�ط��� | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| �縺��ֵ | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
��2����ͼ������֪��ͬһ����Ԫ��ԭ�ӵĵ�һ������I1�仯�����Ǵ��ϵ������μ�С��
��3��ͼ�е�һ��������С��Ԫ�������ڱ��е�λ���ǵ�������IA�壮
��4�����ݶԽ��߹����롢��Ԫ������������Ӧˮ������������ƣ����Ƕ��������ԣ�����Be��OH��2��ʾ�������ʵ����ӷ���ʽ��Be��OH��2+2H+=Be2++2H2O��Be��OH��2+2OH-=BeO2-+2H2O��
��5��ͨ�������縺��ֵ�仯���ɣ�ȷ��þԪ�ص縺��ֵ����С��Χ0.93��1.57��
��6�������Ԫ�صĵ縺�Ժͽ����ԡ��ǽ����ԵĹ�ϵ�Ƿǽ�����Խǿ���縺��Խ������Խǿ���縺��ԽС��
��7���ӵ縺�ԽǶȣ��ж�AlCl3�����ӻ����ﻹ�ǹ��ۻ������˵�����ɣ���д���жϵķ����ͽ��ۣ�AlԪ�غ�ClԪ�صĵ縺�Բ�ֵΪ1.55��1.7�������γɹ��ۼ���Ϊ���ۻ����
�����һ��ʵ�鷽��֤���������õ��Ľ��۽��Ȼ������ȵ�����̬�����е�����ʵ�飬��������磬˵���ǹ��ۻ����
| Ԫ�� | X | Y | Z | W |
| ԭ�Ӱ뾶/nm | 0.037 | 0.075 | 0.074 | 0.099 |
| A�� | Y��Z��W�������ڱ���ͬһ���� | B�� | ͨ��״���µò���������YZ2 | ||
| C�� | X��Z�γɵĻ����ﲻ���Ǽ��Լ� | D�� | X��Z��W�γɵĻ�����Ϊ���� |
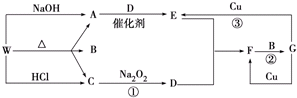
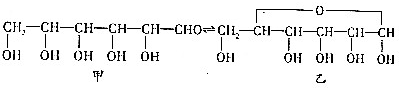
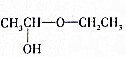 ��д�������ּ��л���ϳɸ������ѵĻ�ѧ����ʽ��CH3CHO+CH3CH2OH��
��д�������ּ��л���ϳɸ������ѵĻ�ѧ����ʽ��CH3CHO+CH3CH2OH��