题目内容
15.溶液体积和pH都相同的一元强酸X与一元弱酸溶液Y,已知弱酸的电离度为0.5%,则X和Y溶液分别中和相同浓度的NaOH溶液时,所需Y溶液的体积是X溶液的( )| A. | 20倍 | B. | 100倍 | C. | 200倍 | D. | 500倍 |
分析 两溶液的pH相同,则氢离子浓度相同,设氢离子浓度为n,一元强酸的物质的量为n,弱酸的物质的量为:$\frac{n}{0.5%}$=200n,然后结合中和反应实质计算出消耗X、Y溶液体积关系,据此进行解答.
解答 解:溶液体积和pH都相同的一元强酸X与一元弱酸溶液Y,两溶液的pH相同,则氢离子浓度相同,设氢离子浓度为n,一元强酸的物质的量为n,该一元弱酸的物质的量为:$\frac{n}{0.5%}$=200n,
设NaOH溶液浓度为c,则X消耗氢氧化钠溶液的体积为:$\frac{n}{c}$,Y消耗氢氧化钠溶液体积为:$\frac{200n}{c}$,
所需Y溶液的体积是X溶液的倍数为:$\frac{\frac{200n}{c}}{\frac{n}{c}}$=200,
故选C.
点评 本题考查了弱电解质的电离平衡,题目难度不大,正确判断两溶液的浓度关系为解答关键,注意掌握弱电解质的电离平衡及其影响,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
6.如表实验操作正确的是( )
| 实验 | 操作 | |
| A | 观察钠与水反应的现象 | 用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| B | 检验NaHCO3与Na2CO3溶液 | 用小试管分别取少量溶液,然后滴加澄清石灰水 |
| C | 证明Na2O2与CO2是放热反应 | Na2O2用棉花包裹,放入充满CO2的集气瓶中,棉花燃烧说明是放热反应 |
| D | 检验Na2CO3与K2CO3溶液 | 用稀硫酸清洗过的铂丝分别蘸取溶液,在酒精灯外焰上灼烧,透过蓝色钴玻璃观察火焰的颜色 |
| A. | A | B. | B | C. | C | D. | D |
3.用2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O反应制取Cl2,被氧化的HCl和未被氧化的HCl的质量之比为( )
| A. | 1:8 | B. | 2:5 | C. | 5:2 | D. | 5:3 |
20.pH=5的NH4Cl溶液由水电离出来的H+离子浓度为a mol•L-1,pH=5的HCOOH溶液由水电离出来的H+离子浓度为b mol•L-1,下列a和b的关系正确的是( )
| A. | a=b | B. | a=10-4b | C. | a=104b | D. | 无法确定 |
7.一包NH4Cl化肥中混入少量其他氮肥,可能是NH4NO3或(NH4)2SO4中的一种,经测定知样品中含氮量为25.7%.这包化肥中氯化铵的质量分数为( )
| A. | 80% | B. | 85% | C. | 90% | D. | 95% |
4.已知:CH3CH2CH2CH3(g)+6.5O2(g)→4CO2(g)+5H2O(l),1mol CH3CH2CH2CH3完全燃烧放出 2878kJ热量;(CH3)2CHCH3(g)+6.5O2(g)→4CO2(g)+5H2O(l),1mol(CH3)2CHCH3燃烧放出2869kJ热量.下列说法正确的是( )
| A. | 1 mol CH3CH2CH2CH3分子储存的能量大于1 mol (CH3)2CHCH3分子 | |
| B. | 1 mol CH3CH2CH2CH3分子储存的能量小于1 mol (CH3)2CHCH3分子 | |
| C. | (CH3)2CHCH3转化为CH3CH2CH2CH3的过程是一个放热过程 | |
| D. | 断开1 mol物质中化学键吸收的能量CH3CH2CH2CH3大于(CH3)2CHCH3 |
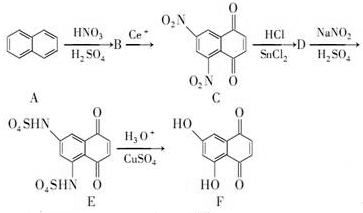
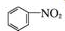 +SnCl2$\stackrel{HCl}{→}$
+SnCl2$\stackrel{HCl}{→}$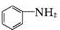 +SnCl4
+SnCl4 .
.