题目内容
7.一包NH4Cl化肥中混入少量其他氮肥,可能是NH4NO3或(NH4)2SO4中的一种,经测定知样品中含氮量为25.7%.这包化肥中氯化铵的质量分数为( )| A. | 80% | B. | 85% | C. | 90% | D. | 95% |
分析 NH4Cl、NH4NO3、(NH4)2SO4的含氮量分别为26.2%、35%、21.2%,根据含氮量可知,混入的氮肥是(NH4)2SO4,根据十字交叉法来求解.
解答 解:NH4Cl、NH4NO3、(NH4)2SO4的含氮量分别为26.2%、35%、21.2%,而样品中含氮量为25.7%,故根据含氮量可知,混入
的氮肥是(NH4)2SO4,根据质量分数十字交叉法 可知,则氯化铵的质量分数为w(NH4Cl)=90%,
可知,则氯化铵的质量分数为w(NH4Cl)=90%,
故选C.
点评 本题考查了混合物成分的判断和根据十字交叉法来计算质量分数,难度不大,注意解题技巧的运用.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
18.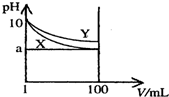 常温下,pH=10的X、Y两种碱溶液各1mL,分别稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,pH=10的X、Y两种碱溶液各1mL,分别稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
 常温下,pH=10的X、Y两种碱溶液各1mL,分别稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,pH=10的X、Y两种碱溶液各1mL,分别稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )| A. | Y碱溶液稀释过程中溶液中c(H+)减小 | |
| B. | 稀释后,X溶液的碱性比Y溶液的碱性弱 | |
| C. | 分别完全中和X、Y这两种碱溶液时,消耗同浓度盐酸的体积VX>VY | |
| D. | 若8<a<10,则X、Y都是弱碱 |
15.溶液体积和pH都相同的一元强酸X与一元弱酸溶液Y,已知弱酸的电离度为0.5%,则X和Y溶液分别中和相同浓度的NaOH溶液时,所需Y溶液的体积是X溶液的( )
| A. | 20倍 | B. | 100倍 | C. | 200倍 | D. | 500倍 |
2.下列说法错误的是( )
| A. | 化学反应实质是旧键断裂新键形成,化学反应中的能量变化本质原因就是旧键断裂所吸收的能量和新键形成所释放的能量不同 | |
| B. | 极性键就是共用电子对发生偏移的共价键 | |
| C. | 氢键是一种比较弱的化学键 | |
| D. | 水结冰时体积膨胀、密度减小就是因为氢键的存在 |
19.将Mg和Cu组成的混合物7.64g投入足量的稀硝酸中使其完全反应,得到的唯一还原产物NO在标准状况下体积为2.24L.将反应后的溶液稀释为1L,测得溶液的pH=1,此时溶液中NO3-的浓度为( )
| A. | 0.3 mol/L | B. | 0.4 mol/L | C. | 0.5 mol/L | D. | 0.6 mol/L |
17.光纤通信是一种现代化的通信手段,制造光导纤维的主要原料是SiO2,下列关于SiO2的说法正确的是( )
| A. | SiO2的摩尔质量是60 | |
| B. | 1mol SiO2中含有1mol O2 | |
| C. | 1.5mol SiO2中含有1.806×1024个氧原子 | |
| D. | 1mol SiO2的质量是60g•mol-1 |
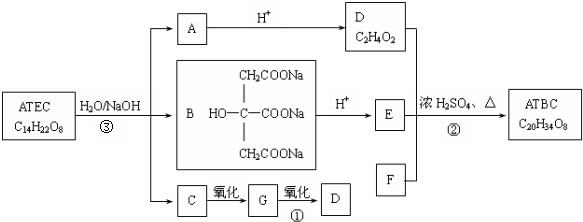
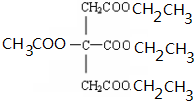 +NaOH$\stackrel{△}{→}$CH3COONa+
+NaOH$\stackrel{△}{→}$CH3COONa+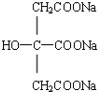 +3CH3CH2OH+3H2O.
+3CH3CH2OH+3H2O.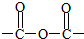 ,E分子在浓硫酸、加热条件下可生成分子甲,其分子式为C6H6O6,则符合上述条件甲分子有2种.
,E分子在浓硫酸、加热条件下可生成分子甲,其分子式为C6H6O6,则符合上述条件甲分子有2种. 某研究性学习小组设计了一组实验验证元素周期律.
某研究性学习小组设计了一组实验验证元素周期律.