题目内容
7.下列有关离子的检验及结论正确的是( )| A. | 用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,说明溶液中含有K+ | |
| B. | 向某无色溶液中滴加BaCl2溶液有白色沉淀出现,说明该溶液中一定含有SO42- | |
| C. | 向某溶液中加AgNO3溶液和稀盐酸,有白色沉淀出现,说明该溶液中一定含有Cl- | |
| D. | 向某溶液中加NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,说明该溶液中一定含有NH4+ |
分析 A.钠的焰色反应为黄色;
B.白色沉淀可能为AgCl;
C.检验氯离子,应先加硝酸,再加硝酸银;
D.产生能使湿润的红色石蕊试纸变蓝的气体,气体为氨气.
解答 解:A.钠的焰色反应为黄色,则用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,说明溶液中含有Na+,故A错误;
B.白色沉淀可能为AgCl,则不能确定是否含SO42-、Cl-,故B错误;
C.检验氯离子,应先加硝酸,再加硝酸银,且加盐酸引入Cl-,不能检验是否含Cl-,故C错误;
D.产生能使湿润的红色石蕊试纸变蓝的气体,气体为氨气,则该溶液中一定含有NH4+,故D正确;
故选D.
点评 本题考查常见离子的检验,为高频考点,把握常见离子的检验方法、试剂与现象等为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
18.“轻轨电车”是近年新兴的一种交通工具.电车开动时,在电车与架空电线的接触点上,由于高速摩擦会产生高温,因此接触点上的材料应该具有耐高温、能导电的性质.对于该接触点上的材料选择,你认为较合适的是( )
| A. | 金刚石 | B. | 石墨 | C. | 铜 | D. | 铁 |
2.下列有关物质用途的说法中,不正确的是( )
| A. | 明矾可作净水剂 | |
| B. | 硅可制作半导体材料 | |
| C. | 氢氧化钠常用于中和胃酸 | |
| D. | 常温下,铁制容器可用于盛装浓硫酸 |
13. 甲、乙、丙、丁、戊五种物质中,甲、乙、丙均含有相同的某种元素,丁是一种常见气体单质,它们之间具有如图所示转化关系.下列有关物质的推断不正确的是( )
甲、乙、丙、丁、戊五种物质中,甲、乙、丙均含有相同的某种元素,丁是一种常见气体单质,它们之间具有如图所示转化关系.下列有关物质的推断不正确的是( )
 甲、乙、丙、丁、戊五种物质中,甲、乙、丙均含有相同的某种元素,丁是一种常见气体单质,它们之间具有如图所示转化关系.下列有关物质的推断不正确的是( )
甲、乙、丙、丁、戊五种物质中,甲、乙、丙均含有相同的某种元素,丁是一种常见气体单质,它们之间具有如图所示转化关系.下列有关物质的推断不正确的是( )| A. | 若甲为Na,则戊可能是H2O | B. | 若甲为C2H4,则戊可能是O2 | ||
| C. | 若甲为NO,则戊可能是H2O | D. | 若甲为Cl2,则戊可能是NaOH溶液 |
14.电解质电离要吸收能量,用50mL0.1mol•L-1的盐酸分别与60mL0.1mol•L-1NaOH溶液、60mL0.1mol•L-1氨水充分反应,放出热量( )
| A. | 相等 | B. | 前者大于后者 | C. | 后者大于前者 | D. | 无法判断 |
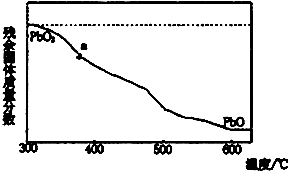 (1)某小组分析二氧化铅分解产物的组成,取478g的PbO2加热,PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a为96.66%,则a点固体的分子式为Pb2O3
(1)某小组分析二氧化铅分解产物的组成,取478g的PbO2加热,PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a为96.66%,则a点固体的分子式为Pb2O3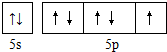 .
.