题目内容
2.下列有关物质用途的说法中,不正确的是( )| A. | 明矾可作净水剂 | |
| B. | 硅可制作半导体材料 | |
| C. | 氢氧化钠常用于中和胃酸 | |
| D. | 常温下,铁制容器可用于盛装浓硫酸 |
分析 A.明矾水解生成具有吸附性的胶体;
B.Si位于金属与非金属的交界处,具有金属性和非金属性;
C.氢氧化钠为强碱,具有强腐蚀性;
D.常温下,Fe遇浓硫酸发生钝化.
解答 解:A.明矾水解生成具有吸附性的胶体,则明矾可作净水剂,吸附水中的悬浮杂质,故A正确;
B.Si位于金属与非金属的交界处,具有金属性和非金属性,则硅可制作半导体材料,故B正确;
C.氢氧化钠为强碱,具有强腐蚀性,不能中和胃酸,可选氢氧化铝、碳酸氢钠中和,故C错误;
D.常温下,Fe遇浓硫酸发生钝化,则常温下,铁制容器可用于盛装浓硫酸,故D正确;
故选C.
点评 本题考查物质的性质、应用,为高频考点,把握物质的性质、化学与生活、性质与用途等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
12.下列条件下,两瓶气体所含原子数、分子数一定相等的是( )
| A. | 同质量、不同密度的N2和CO | B. | 同密度、同体积的H2和N2 | ||
| C. | 同体积、同密度的C2H4和C3H6 | D. | 同温度、同体积的N2O和CO2 |
13.以下事实不能用元素周期律解释的是( )
| A. | F2在暗处遇H2即爆炸,I2在暗处遇H2几乎不反应 | |
| B. | H2O在4000℃以上开始明显分解,H2S用酒精灯加热即可完全分解 | |
| C. | 氯与钠形成离子键,氯与硅形成共价键 | |
| D. | “NO2球”在冷水中颜色变浅,在热水中颜色加深 |
10.新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,价电子的电子排布式3s23p5,价电子所在电子层的轨道数9.
②LiBH4由Li+和BH4-构成,BH4-的空间构型是正四面体,B原子的杂化轨道类型是sp3.
③Li、B元素的第一电离能由大到小排列顺序为B>Li.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+<H-(填“>”、“=”或“<”).
②某储氢材料是短周期金属元素M的氢化物.M的部分电离能如下表所示:
M是Mg(填元素符号).
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞边长a=480pm,Na+半径为104pm,H-的半径为136pm,NaH的理论密度是$\frac{96}{(4.8×1{0}^{-8})^{3}{N}_{A}}$g•cm-3.(用NA表示)
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,价电子的电子排布式3s23p5,价电子所在电子层的轨道数9.
②LiBH4由Li+和BH4-构成,BH4-的空间构型是正四面体,B原子的杂化轨道类型是sp3.
③Li、B元素的第一电离能由大到小排列顺序为B>Li.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径:Li+<H-(填“>”、“=”或“<”).
②某储氢材料是短周期金属元素M的氢化物.M的部分电离能如下表所示:
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞边长a=480pm,Na+半径为104pm,H-的半径为136pm,NaH的理论密度是$\frac{96}{(4.8×1{0}^{-8})^{3}{N}_{A}}$g•cm-3.(用NA表示)
7.下列有关离子的检验及结论正确的是( )
| A. | 用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,说明溶液中含有K+ | |
| B. | 向某无色溶液中滴加BaCl2溶液有白色沉淀出现,说明该溶液中一定含有SO42- | |
| C. | 向某溶液中加AgNO3溶液和稀盐酸,有白色沉淀出现,说明该溶液中一定含有Cl- | |
| D. | 向某溶液中加NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,说明该溶液中一定含有NH4+ |
14.具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的说法正确的是( )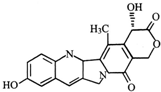

| A. | 该物质属于芳香烃 | |
| B. | 该物质能与NaHCO3反应 | |
| C. | 该物质中存在三个苯环 | |
| D. | 一定条件下,1mol该物质最多可与2mol NaOH发生反应 |
9.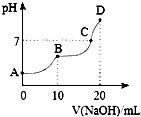 25℃时,向10mL 0.1mol•L-1 H2C2O4溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述不正确的是( )
25℃时,向10mL 0.1mol•L-1 H2C2O4溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述不正确的是( )
 25℃时,向10mL 0.1mol•L-1 H2C2O4溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述不正确的是( )
25℃时,向10mL 0.1mol•L-1 H2C2O4溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列叙述不正确的是( )| A. | C点溶液中含有NaHC2O4和Na2C2O4 | |
| B. | NaHC2O4溶液中水的电离程度比Na2C2O4溶液中小 | |
| C. | B点,c (Na+)=2[c (H2C2O4)+c (HC2O4-)+c (C2O42-)] | |
| D. | D点,c (Na+)>c (C2O42-)>c (OH-)>c (HC2O4-)>c (H+) |