题目内容
12.碳及其化合物广泛存在于自然界中,回答下列问题:(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用形象化描述电子云.
(2)碳在形成化合物时,其键型以共价键为主,原因是C有4个价电子且半径较小,难以通过得或失电子达到稳定结构.
(3)C2H2 分子中,共价键的类型有σ键、π键,C 原子的杂化轨道类型是SP,写出两个与C2H2 具有相
同空间构型含碳无机物分子的分子式CO2.
( 4 )CO 能与金属Fe、Ni 分别形成Fe(CO)5、Ni(CO)4,Fe(CO)5 中Fe 元素的原子核外电子排布
为1s22s22p63s23p63d64s2,Ni(CO)4 是无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂推测Ni(CO)4 是分子晶体.
(5)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C 原子连接3个六元环,每个六元环占有2个C 原子.
②在金刚石晶体中,C 原子所连接的最小环也为六元环,每个C 原子连接12个六元环,六元环中最
多有4个C 原子在同一平面.
分析 (1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用电子云形象化描述;
(2)共价键为原子之间以共用电子对成键,碳的非金属性较弱,但半径较小,反应中难以失去或得到电子;
(3)单键为σ键,双键和三键中均含σ键、π键;结合σ键和孤对电子数判断价层电子对数,以此判断杂化类型;
(4)根据铁元素的质子数可知电子数为26,核外各电子层电子数为2、8、14、2,分子晶体的熔沸点较低;
(5)①石墨晶体中最小的环为六元环,每个碳原子连接3个C-C化学健,每个C-C化学健被2个碳原子共用;
②在金刚石的晶体结构中每个碳原子与周围的4个碳原子形成四个碳碳单键,这5个碳原子形成的是正四面体结构,键角为109028,最小的环为6元环.
解答 解:(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用电子云形象化描述,离核近的区域电子云密度较大,离核远的区域电子云密度较小,
故答案为:电子云;
(2)共价键为原子之间以共用电子对成键,碳原子核外有4个电子,且元素的非金属性较弱,但半径较小,反应中难以失去或得到电子,
故答案为:C有4个价电子且半径较小,难以通过得或失电子达到稳定结构;
(3)乙炔的结构式为H-C≡C-H,C2H2中存在C≡C,则既有σ键又有π键,分子中C原子形成2个σ键,孤对电子数为$\frac{4-2×2}{2}$=0,则为sp杂化,为直线形结构;CO2分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+$\frac{1}{2}$(4-2×2)=2,所以二氧化碳是直线型结构,二氧化碳属于无机物,
故答案为:σ键、π键;sp;CO2;
(4)铁元素的质子数为26,核外各电子层电子数为2、8、14、2,其原子基态时的核外电子排布式为1s22s22p63s23p63d64s2,分子晶体的熔沸点较低,四羰基镍熔点-19.3℃,沸点42.1℃,所以该物质为分子晶体,
故答案为:1s22s22p63s23p63d64s2;分子;
(5)①石墨晶体中最小的环为六元环,每个碳原子连接3个C-C化学健,则每个C原子连接 3个六元环,每个六元环占有的C原子数为6×$\frac{1}{3}$=2,
故答案为:3;2;
②在金刚石的晶体结构中每个碳原子与周围的4个碳原子形成四个碳碳单键,最小的环为6元环,每个单键为3个环共有,则每个C原子连接4×3=12个六元环,晶胞中共平面的原子如图 ,共4个,
,共4个,
故答案为:12;4.
点评 本题主要考查物质结构和性质,侧重考查学生空间想象能力、知识运用能力,涉及原子核外电子排布、晶胞计算等知识点,综合性较强,采用均摊法、价层电子对互斥理论等理论分析解答,题目难度中等.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案| A. | 食品包装内常放置具有吸水性的化学药品以保持干燥,如五氧化二磷和硅胶 | |
| B. | 青蒿素在超临界CO2中有很强的溶解性,萃取青蒿素可用超临界CO2作萃取剂 | |
| C. | 利用太阳能电池板发电,不发生化学变化 | |
| D. | 在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 |
| A. | 用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,说明溶液中含有K+ | |
| B. | 向某无色溶液中滴加BaCl2溶液有白色沉淀出现,说明该溶液中一定含有SO42- | |
| C. | 向某溶液中加AgNO3溶液和稀盐酸,有白色沉淀出现,说明该溶液中一定含有Cl- | |
| D. | 向某溶液中加NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,说明该溶液中一定含有NH4+ |
| A. | 常温下,相同浓度的盐酸与氨水的混合溶液的pH=7,消耗盐酸的体积大 | |
| B. | 将pH=5的醋酸溶液稀释1000倍,溶液的pH=8 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| A. | 18g D2O含有电子数为10NA | |
| B. | 常温下,4.6 g Na和足量的O2完全反应失去电子数为0.2NA | |
| C. | 标准状况下,11.2 LNO和11.2 L O2混合后气体的分子总数为NA | |
| D. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| A. | 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O═HClO+HSO3- | |
| B. | 向AlCl3溶液中投入过量Na:Al3++4Na+2H2O═AlO2-+4Na++2H2↑ | |
| C. | 向FeBr2溶液中通入少量Cl2:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-完全沉淀:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4 |
 .
. .
.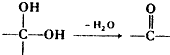
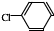 中氯原子较难水解
中氯原子较难水解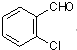 )可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式
)可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式 、
、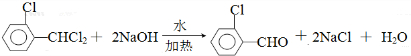 .该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式
.该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式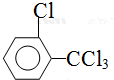 、
、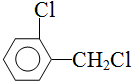 .
.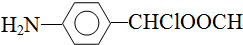 .
.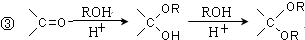
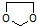 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: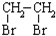
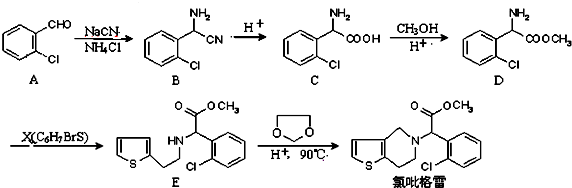
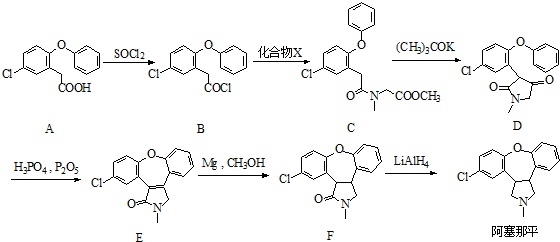
 )是临床上一种降脂抗血栓药物,它的一条合成路线如下:
)是临床上一种降脂抗血栓药物,它的一条合成路线如下:

 .
. .
.
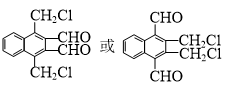 .
.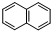 )的衍生物,且取代基都在同一个苯环上;
)的衍生物,且取代基都在同一个苯环上;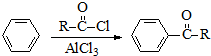 (R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和
(R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和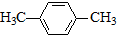 为原料制备
为原料制备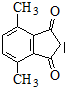 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下: