题目内容
17.常温下,下列各组离子一定能在指定溶液中大量共存的是( )| A. | 使酚酞呈红色的溶液:Na+、NH4+、Al3+、NO3- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=0.1mol•L-1的溶液:Na+、K+、CO32-、ClO- | |
| C. | 含有Fe3+的溶液:Na+、Al3+、Cl-、SCN- | |
| D. | 由水电离产生的c(OH-)=1×10-14mol•L-1溶液:K+、Na+、Cl-、HCO3- |
分析 A.使酚酞呈红色的溶液中存在大量氢氧根离子,铵根离子、铝离子与氢氧根离子反应;
B.该溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
C.铁离子与硫氰根离子反应生成硫氰化铁;
D.由水电离产生的c(OH-)=1×10-14mol•L-1溶液中存在大量氢离子或氢氧根离子,碳酸氢根离子与氢离子和氢氧根离子反应.
解答 解:A.使酚酞呈红色的溶液为碱性溶液,溶液中存在大量氢氧根离子,NH4+、Al3+与氢氧根离子反应,在溶液中不能大量共存,故A错误;
B.该溶液为碱性溶液,溶液中存在大量氢氧根离子,Na+、K+、CO32-、ClO-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.Fe3+、SCN-之间反应生成络合物硫氰化铁,在溶液中不能大量共存,故C错误;
D.由水电离产生的c(OH-)=1×10-14mol•L-1溶液为酸性或碱性溶液,溶液中存在电离氢离子或氢氧根离子,HCO3-与氢离子、氢氧根离子反应,在溶液中一定不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:

环己醇、环己酮和水的部分物理性质见下表:
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多.实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧瓶中,在55-60℃进行反应.反应完成后,加入适量水,蒸馏,收集95-100℃的馏分,得到主要的含环己酮和水的混合物.
①酸性Na2Cr2O7溶液的加料方式为缓慢滴加.
②蒸馏不能分离环己酮和水的原因是环已酮和水形成具有固定组成的混合物一起蒸出.
(2)环己酮的提纯需要经过以下一系列的操作:
a蒸馏,收集151-156℃的馏分;b 过滤;c 在收集到的馏分中加NaCl固体至饱和,静置,分液;d 加入无水MgSO4固体,除去有机物中少量水.
①上述操作的正确顺序是cdba(填字母).
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需漏斗、分液漏斗.
③在上述操作c中,加入NaCl固体的作用是增加水层的密度,有利于分层.
(3)利用红外光谱图,可确定环己酮分子含官能团名称羰基.

环己醇、环己酮和水的部分物理性质见下表:
| 物质 | 沸点(℃) | 密度(g-cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95)* | 0.9478 | 微溶于水 |
| 水 | 100.0 | 0.9982 |
(1)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多.实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧瓶中,在55-60℃进行反应.反应完成后,加入适量水,蒸馏,收集95-100℃的馏分,得到主要的含环己酮和水的混合物.
①酸性Na2Cr2O7溶液的加料方式为缓慢滴加.
②蒸馏不能分离环己酮和水的原因是环已酮和水形成具有固定组成的混合物一起蒸出.
(2)环己酮的提纯需要经过以下一系列的操作:
a蒸馏,收集151-156℃的馏分;b 过滤;c 在收集到的馏分中加NaCl固体至饱和,静置,分液;d 加入无水MgSO4固体,除去有机物中少量水.
①上述操作的正确顺序是cdba(填字母).
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需漏斗、分液漏斗.
③在上述操作c中,加入NaCl固体的作用是增加水层的密度,有利于分层.
(3)利用红外光谱图,可确定环己酮分子含官能团名称羰基.
6.下列离子方程式正确的是( )
| A. | 在海带灰的滤液中加入几滴稀硫酸,再加入双氧水,即能使淀粉溶液变蓝2I-+H2O2+2H+═I2+2H2O | |
| B. | Na2S2O3溶液中加入稀硫酸:2S2O32-+2H+═SO42-+3S↓+H2O | |
| C. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ | |
| D. | 在AgCl饱和溶液在加入Na2S:2Ag++S2-═Ag2S↓ |
7.在水溶液中能大量共存的离子组是( )
| A. | Mg2+、Cl-、OH- | B. | Na+、CO32-、OH- | C. | Fe2+、H+、CO32- | D. | Fe3+、K+、OH- |
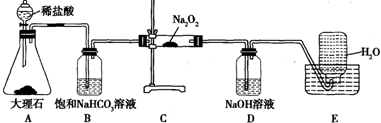
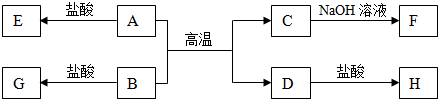
 .
.